题目内容
【题目】用98%浓硫酸配制0.1mol/L的稀硫酸,下列情况会使所配溶液浓度偏低的是( )
A.未冷却就转移、定容
B.容量瓶内原有少量蒸馏水
C.定容时俯视刻度线观察液面
D.定容时加多了水再用吸管吸出
【答案】D
【解析】解:A.未冷却就转移、定容,V偏小,由c= ![]() 可知,浓度偏高,故A不选;B.容量瓶内原有少量蒸馏水,对实验无影响,故B不选;
可知,浓度偏高,故A不选;B.容量瓶内原有少量蒸馏水,对实验无影响,故B不选;
C.定容时俯视刻度线观察液面,V偏小,由c= ![]() 可知,浓度偏高,故C不选;
可知,浓度偏高,故C不选;
D.定容时加多了水再用吸管吸出,V偏大,由c= ![]() 可知,则使所配溶液浓度偏低,故D选;
可知,则使所配溶液浓度偏低,故D选;
故选D.
【考点精析】关于本题考查的配制一定物质的量浓度的溶液,需要了解配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用交投滴管加水至刻度线才能得出正确答案.

【题目】某小组同学为探究物质的氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。
已知:①溴水为溴的水溶液,溴水为橙黄色,溴蒸气为红棕色,均有毒
②氯水为氯气的水溶液。
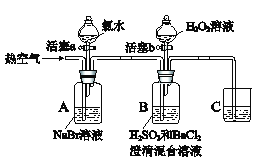
实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为橙黄色 |
Ⅱ | 吹入热空气 | A中橙黄色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成橙黄色 |
请回答下列问题:
(1)A中反应的离子方程式是__________________________________________。
(2)实验操作II吹入热空气的目的是___________________________________。
(3)装置C的作用是_____________________________________。
(4)实验操作III,混合液逐渐变成橙黄色,其对应的离子方程式是____________。
(5)由操作I得出的结论是_____________,由操作III得出的结论是______________。
(6)实验反思:实验操作III,开始时颜色无明显变化的原因是(写出一条即可):___________。