题目内容
化学方程式可简明地体现元素及其化合物的性质.已知:
氧化还原反应:
FeCl3+H2S═FeCl2+S;PbO2+4HCl=PbCl2+Cl2↑+2H2O
2Fe(OH)2+Cl2+2KOH═2Fe(OH)3+2KCl;Cl2+2KOH=KCl+KClO+H2O
水溶液中的复分解反应:(Se元素的原子序数为34)
CuSO4+H2S=CuS↓+H2SO4;H2SeO4+2NaN3=Na2SeO4+2HN3;HN3+Na2S=NaN3+H2S
热分解反应:
BaCO3 BaO+CO2↑;MgCO3
BaO+CO2↑;MgCO3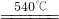 MgO+CO2↑;CuCO3
MgO+CO2↑;CuCO3 CuO+CO2↑
CuO+CO2↑
下列说法不正确的是
- A.氧化性(酸性溶液):PbO2>Fe3+>S
- B.还原性(碱性溶液):Fe(OH)2>KCl>Cl2
- C.酸性(水溶液):H2S>H2SO4>H2SeO4>HN3
- D.热稳定性:BaCO3>MgCO3>CuCO3
C
分析:A.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
B.自发进行的氧化还原反应中,还原剂的还原性大于还原产物的还原性;
C.硫酸的酸性大于硫化氢;
D.分解温度越高,该物质越稳定.
解答:A.FeCl3+H2S═FeCl2+S中氧化性:Fe3+>S,PbO2+4HCl=PbCl2+Cl2↑+2H2O中氧化性PbO2>Cl2,2Fe(OH)2+Cl2+2KOH═2Fe(OH)3+2KCl中氧化性Cl2>Fe3+;Cl2+2KOH=KCl+KClO+H2O中氧化性Cl2>KClO,所以氧化性PbO2>Fe3+>S,故A正确;
B.FeCl3+H2S═FeCl2+S中还原性H2S>FeCl2;PbO2+4 HCl=PbCl2+Cl2↑+2H2O中还原性HCl>PbCl2,2Fe(OH)2+Cl2+2KOH═2Fe(OH)3+2KCl中还原性Fe(OH)2>KCl;Cl2+2KOH=KCl+KClO+H2O中还原性KCl>Cl2,所以还原性Fe(OH)2>KCl>Cl2,故B正确;
C.根据强酸制取弱酸知H2SO4>H2SeO4>HN3,但硫酸是强酸,硫化氢是弱酸,所以硫酸的酸性大于硫化氢,故C错误;
D.分解温度越高,该物质越稳定,所以碳酸盐的稳定性大小顺序是BaCO3>MgCO3>CuCO3,故D正确;
故选C.
点评:本题考查了氧化性、还原性、酸性、热稳定性的判断,根据其规律来分析解答即可,难度不大,注意C选项中,硫化氢能制取硫酸,为特殊反应.
分析:A.自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
B.自发进行的氧化还原反应中,还原剂的还原性大于还原产物的还原性;
C.硫酸的酸性大于硫化氢;
D.分解温度越高,该物质越稳定.
解答:A.FeCl3+H2S═FeCl2+S中氧化性:Fe3+>S,PbO2+4HCl=PbCl2+Cl2↑+2H2O中氧化性PbO2>Cl2,2Fe(OH)2+Cl2+2KOH═2Fe(OH)3+2KCl中氧化性Cl2>Fe3+;Cl2+2KOH=KCl+KClO+H2O中氧化性Cl2>KClO,所以氧化性PbO2>Fe3+>S,故A正确;
B.FeCl3+H2S═FeCl2+S中还原性H2S>FeCl2;PbO2+4 HCl=PbCl2+Cl2↑+2H2O中还原性HCl>PbCl2,2Fe(OH)2+Cl2+2KOH═2Fe(OH)3+2KCl中还原性Fe(OH)2>KCl;Cl2+2KOH=KCl+KClO+H2O中还原性KCl>Cl2,所以还原性Fe(OH)2>KCl>Cl2,故B正确;
C.根据强酸制取弱酸知H2SO4>H2SeO4>HN3,但硫酸是强酸,硫化氢是弱酸,所以硫酸的酸性大于硫化氢,故C错误;
D.分解温度越高,该物质越稳定,所以碳酸盐的稳定性大小顺序是BaCO3>MgCO3>CuCO3,故D正确;
故选C.
点评:本题考查了氧化性、还原性、酸性、热稳定性的判断,根据其规律来分析解答即可,难度不大,注意C选项中,硫化氢能制取硫酸,为特殊反应.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______.
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:______.
(4)⑥的单质与⑤的最高价氧化物的水化物发生反应的化学方程式:______.
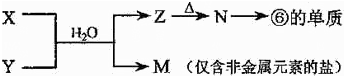
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:X溶液与Y溶液反应的离子方程式为______.