题目内容
(8分)根据下列流程处理废旧电路板,回收金属M,并制得高效绿色净水剂K2EO4。
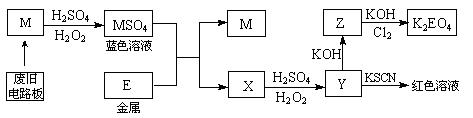
据此回答问题:
(1)M的化学式是 。
 (2)M MSO4过程中,氧化剂是 ,还原剂是 。
(2)M MSO4过程中,氧化剂是 ,还原剂是 。
(3)写出Z→K2EO4的化学反应方程式: 。
(4)向Y溶液中滴加KI淀粉溶液,变为蓝色,其原因用离子方程式解释为: 。
(5)控制其他条件相同,印刷电路板的金属 M用10%H2O2和3.0mol/LH2SO4的混合溶液处理,测得不同温度下金属M的平均溶解速率(见下表)。
当温度高于40℃时,M的平均溶解速率随着反应温度升高而下降,其主要原因是 。

据此回答问题:
(1)M的化学式是 。
 (2)M MSO4过程中,氧化剂是 ,还原剂是 。
(2)M MSO4过程中,氧化剂是 ,还原剂是 。(3)写出Z→K2EO4的化学反应方程式: 。
(4)向Y溶液中滴加KI淀粉溶液,变为蓝色,其原因用离子方程式解释为: 。
(5)控制其他条件相同,印刷电路板的金属 M用10%H2O2和3.0mol/LH2SO4的混合溶液处理,测得不同温度下金属M的平均溶解速率(见下表)。
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| V(M)(x10-3mol.L-1.min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
(8分)
(1) Cu(1分)
(2) H2O2 ,Cu (2分)
(3) 10KOH + 3Cl2 + 2Fe(OH)3 ="=" 2K2FeO4 + 6KCl + 8H2O (2分)
(4) 2Fe3+ + 2I— ="=" 2Fe2+ + I2 (2分)
(5) 过氧化氢分解浓度降低造成速率减慢。(1分)
(1) Cu(1分)
(2) H2O2 ,Cu (2分)
(3) 10KOH + 3Cl2 + 2Fe(OH)3 ="=" 2K2FeO4 + 6KCl + 8H2O (2分)
(4) 2Fe3+ + 2I— ="=" 2Fe2+ + I2 (2分)
(5) 过氧化氢分解浓度降低造成速率减慢。(1分)
略

练习册系列答案
相关题目

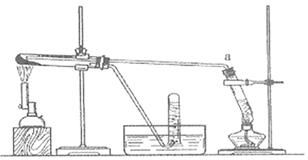
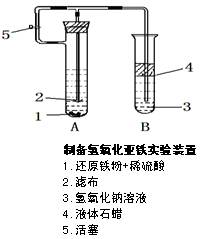
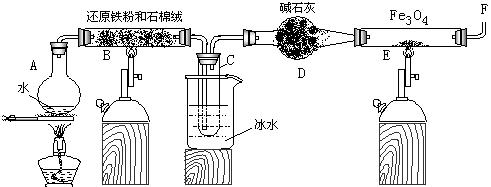
 Fe3O4 +4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释
Fe3O4 +4H2在一定条件下实际上为可逆反应,本实验中是如何实现Fe向Fe3O4的转变的?试用化学平衡移动原理加以解释