��Ŀ����
����Ŀ��A����.���ӹ�ҵ����FeCl3��Һ��ʴ��Ե���ϵ�ͭ��������ӡˢ��·�塣�Ӹ�ʴ��Һ(��Ҫ��FeCl3��FeCl2��CuCl2 )�л���ͭ�������»��FeCl3��Һ����Һ�����������£�
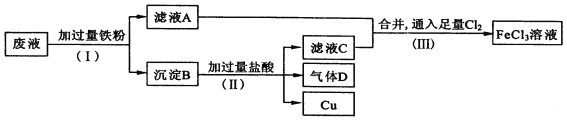
(1)����(��)�з�����Һ�ͳ����IJ���������____________________��
(2)����B����Ҫ��������__________������D��_________________��
(3)д������(��)������FeCl3�Ļ�ѧ����ʽ_____________________________��
(4)ȡ��������������Һ�μ�____________(����KSCN��Һ������ϡ������)����Һ�ʺ�ɫ��֤����Fe3+���ڣ�д���÷�Ӧ�����ӷ���ʽ___________________��
���𰸡����� Cu(��ͭ) H2 (������) 2FeCl2 + Cl2=2FeCl3 KSCN��Һ Fe3+ +3SCN-- = Fe(SCN)3
��������
��ʴ��Һ��Ҫ��FeCl3��FeCl2��CuCl2��ת����ϵͼ��֪:���Һ�м�����������ۣ�������ӦFe+2FeCl3=3FeCl2��Fe+CuCl2= FeCl2 +Cu������ҺAΪFeCl2��Һ������BΪCu��Fe�������B�мӹ������ᣬ������ӦFe+2HCl= FeCl2+H2��������ҺCΪFeCl2��HCl�Ļ����Һ������DΪH2������ҺA����ҺC�ϲ���ͨ��������Cl2��������Ӧ2FeCl2 +Cl2 =2FeCl3��
(1)������(��)�ǽ����������Һ���룬���������ǹ��ˣ�
�ʴ�Ϊ�����ˣ�
(2)������B����Ҫ����Cu��Fe������D��H2��
�ʴ�Ϊ��Cu(��ͭ)��H2 (������)��
(3)������(��) ��FeCl2��Cl2��Ӧ����FeCl3����ѧ����ʽΪ��2FeCl2 + Cl2=2FeCl3��
�ʴ�Ϊ��2FeCl2 + Cl2=2FeCl3��
(4)��Fe3+��KSCN��Һ��죻
�ʴ�Ϊ��KSCN��Һ��Fe3+ +3SCN-- = Fe(SCN)3��

 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д�