��Ŀ����
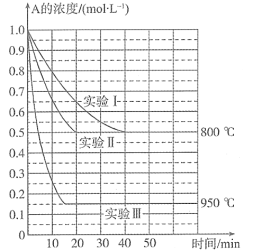
����Ŀ����ͼ��ʾ���ס��ҡ����ֱ��ʾ�ڲ�ͬ�����������淴ӦA(g)+B(g)![]() xC(g)��������C�İٷֺ���w(C)�ͷ�Ӧʱ��(t)�Ĺ�ϵ��
xC(g)��������C�İٷֺ���w(C)�ͷ�Ӧʱ��(t)�Ĺ�ϵ��


��1���������������߷ֱ�����д������������������ ���ߴ�������ʱ�������
��2�����ұ�ʾ��Ӧ�ﵽƽ��״̬�����ֱ��ں��º�ѹ�����ºͺ��º�����������ƽ���������г���He���������� ���߱�ʾ���º��ݵ�������Ҵ�ʱ���������w(C) (������С�����䡱)��
��3�����ݱ������жϸÿ��淴Ӧ������Ӧ�� (����ȡ������ȡ�)��Ӧ��x��ֵΪ ��
��4������ʾ��ij�̶��ݻ����ܱ����������������淴Ӧ�ﵽƽ�����ij���������¶�(T)�ı仯��������������������������������� (�����)��
��w(C) ��A��ת���� ��B��ת���� ��ѹǿ ��c(A) ��c(B)
�����¶���ƽ���� (�����Ӧ�����淴Ӧ��)�����ƶ���
���𰸡���1��b ��2��a ��С ��3������ 1 ��4���٢ڢ� ����Ӧ
����������1��ʹ�ô������Լӿ컯ѧ��Ӧ���������̷�Ӧ����ƽ���ʱ�䡣
��2�����º���ͨ��He����������и����Ũ�ȡ�ѹǿ��������ƽ�ⲻ�����ƶ�������������������������w(C)��С�����º�ѹͨ��He�������ѹǿ��С����Ӧ���ʼ�С������ƽ���ʱ���ӳ���
��3������ͼ����ʾ����ѹ�������������¶���w(C)������˵������ӦΪ���ȷ�Ӧ������������������ѹǿ��w(C)������ƽ��������Ӧ�����ƶ�����x<2������x=1��
��4�����������¶���ƽ��������Ӧ�����ƶ�����w(C)������A��B��ת�������������ϵ��ѹǿ��c(A)��c(B)����С��

 �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�