题目内容
离子化合物的化学式为NH5,它的所有原子的最外电子层都符合相应的稀有气体原子的最外层电子结构。该物质适当受热就能分解生成两种气体。试回答下列问题:(1)固体NH5的电子式为__________________________。
(2)NH5溶于水后,溶液呈___________性(填“酸”“碱”或“中”)。写出NH5与水反应的化学方程式_____________________________。
(3)NH5与铜或铜的某种化合物在一定条件下可生成CuH。CuH是一种难溶物,它能与盐酸反应,生成一种单质气体和一种难溶于水的白色固体。试写出CuH与盐酸反应的化学方程式____________________________。
(1)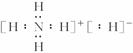
(2)碱
NH4H+H2O====NH3·H2O+H2↑
(3)CuH+HCl====CuCl↓+H2↑
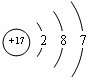
解析:NH5是由1个![]() 原子与5个·H原子作用形成的,分析它们采取何种方式才能实现稳定电子结构,可知NH5应是由
原子与5个·H原子作用形成的,分析它们采取何种方式才能实现稳定电子结构,可知NH5应是由![]() 与H-形成的离子化合物。
与H-形成的离子化合物。
(1)NH5的电子式为 。
。
(2)NH4H溶于水电离出的![]() 、H-与H2O电离出的H+、OH-阴、阳离子重组,
、H-与H2O电离出的H+、OH-阴、阳离子重组,![]() 与OH-组合为NH3·H2O,H-与H+组合后发生氧化还原反应而变为H2,反应的方程式为NH4H+H2O====NH3·H2O+H2↑,所得溶液为氨水,显碱性。(3)CuH与HCl进行阴、阳离子重组,反应方程式为CuH+HCl====CuCl↓+H2↑。
与OH-组合为NH3·H2O,H-与H+组合后发生氧化还原反应而变为H2,反应的方程式为NH4H+H2O====NH3·H2O+H2↑,所得溶液为氨水,显碱性。(3)CuH与HCl进行阴、阳离子重组,反应方程式为CuH+HCl====CuCl↓+H2↑。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
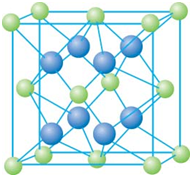 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B.请回答:
已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B形成的晶体其晶胞结构如图,图中小球代表D,大球代表B.请回答: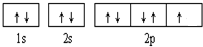
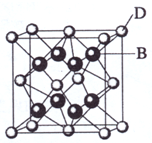 (2009?海南)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图.
(2009?海南)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第7列元素.D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图. 已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大.A与其他4种元素既不在同一周期又不在同一族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第8列元素.D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如图.请回答:
已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大.A与其他4种元素既不在同一周期又不在同一族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第8列元素.D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如图.请回答: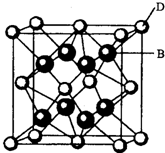 【化学一一选修物质结构与性质】
【化学一一选修物质结构与性质】