题目内容
【题目】(1)画出下列元素的原子结构示意图。
①核电荷数为13的元素:_______。
②最外层电子数等于次外层电子数的元素原子:______。
(2)现有粒子:1H、35Cl、2H、14N、2H37Cl,其中:
①有_________种元素;
②__________之间互称同位素。
【答案】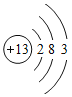
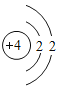 、
、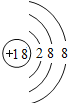 3 1H、2H
3 1H、2H
【解析】
(1)①核电荷数为13的元素为铝元素,其原子结构示意图为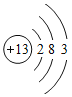 ,故答案为:
,故答案为: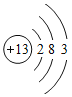 :
:
②最外层电子数等于次外层电子数的元素原子有铍元素、氩元素,其原子结构示意图分别为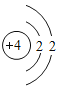 、
、 ,故答案为:
,故答案为: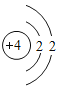 、
、 ;
;
(2)1H、2H质子数相同,中子数不同,互为同位素,35Cl为氯元素的一种核素,14N为氮元的一种核素,2H37Cl为氯化氢,由此可知,有3种元素,一种物质,故答案为:3;1H、2H。

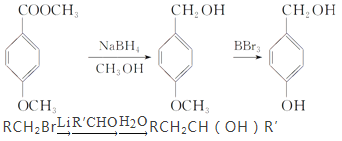
【题目】(16分)工业上可以在恒容密闭容器中采用下列反应制备甲醇:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
(1)下列情况可以作为判断反应达到平衡状态的依据的是(填序号) 。
A.生成CH3OH 的速率与消耗H2的速率之比为1︰2
B.混合气体的平均相对分子质量保持不变
C.混合气体的密度保持不变
D.体系内的压强保持不变
(2)下表所列数据为该反应在不同温度下的化学平衡常数:
温度/℃ | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
①反应的平衡常数表达式为K= 。由上表数据判断,该反应的△H 0(填“>”、“=”或“<”)。升高温度,正反应速率 (填“增大”、“减小”或“不变”)。
②某温度下,将2molCO和6molH2充入一个容积为2L的密闭容器中,达到平衡时c(H2)=1.4mol/L,则CO的转化率为 ,此时的温度为 。
(3)欲提高CO的转化率,可采取的措施是 。(填序号)
A.升温
B.加入更高效的催化剂
C.恒容条件下充入CO
D.恒容条件下充入H2
E.恒容条件下充入氦气
F.及时移走CH3OH
(4)一定条件下,CO和H2在催化剂作用下生成1molCH3OH的能量变化为90.8kJ。该温度下,在三个容积相同的密闭容器中,按不同方式投料,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 | |
投料方式 | 1molCO、2molH2 | 1molCH3OH | 2molCH3OH | |
平衡数据 | C(CH3OH)/(mol/L) | c1 | c2 | c3 |
体系压强(Pa) | p1 | p2 | p3 | |
反应的能量变化 | akJ | bkJ | ckJ | |
原料转化率 | α1 | α2 | α3 | |
下列分析正确的是 。(填序号)
A.2c1<c3 B.2 p1<p3C.|a|+|b|=90.8 D.α1+α3>1
【题目】有A、B、C、D、E五种短周期元素,其元素特征信息如下表
元素 | 元素特征信息 |
A | 其单质是密度最小的物质。 |
B | 阴离子带两个单位负电荷,单质是空气的主要成分之一。 |
C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物。 |
D | 其氢氧化物和氧化物都有两性,与C同周期 |
E | 与C同周期,原子半径在该周期最小 |
回答下列问题:
(1)写出下列元素的名称:C___________,E______________
(2)写出A、B、C形成的化合物的电子式____________________
(3)B、C、D的简单离子半径由大到小的顺序是(用化学式表示)____________________
(4)写出E单质与A、B、C形成的化合物反应的化学方程式:__________________________