题目内容
【题目】(1)甲醇是一种重要的化工产品,可利用甲醇催化脱氢制备甲醛。甲醛与气态甲醇转化的能量关系如图所示。

反应过程中的能量关系
①甲醇催化脱氢转化为甲醛的反应是________(填“吸热”或“放热”)反应。
②过程Ⅰ与过程Ⅱ的反应热是否相同?____________原因是_______________。
③写出甲醇催化脱氢转化为甲醛的热化学反应方程式_________________________________。
(2)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
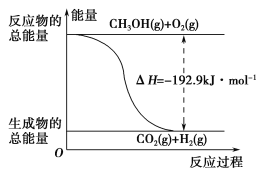
②CH3OH(g)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
下列说法正确的是________。
A.CH3OH转变成H2的过程一定要吸收能量
B.①反应中,反应物的总能量高于生成物的总能量
C.根据②推知反应:CH3OH(l)+![]() O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1
D.反应②的能量变化如图所示
【答案】(1)①吸热 ②相同 一个化学反应的反应热仅与反应始态和终态有关,而与反应的途径无关 ③CH3OH(g)![]() HCHO(g)+H2(g) ΔH=+(E2-E1)kJ·mol-1(2)C
HCHO(g)+H2(g) ΔH=+(E2-E1)kJ·mol-1(2)C
【解析】
(1)①E1<E2,甲醇催化脱氢转化为甲醛的反应是吸热反应。②反应热与反应的始态和终态有关,与反应的途径无关,故反应热相同。
(2)采用反应①将CH3OH转变成H2时,反应吸热,采用反应②将CH3OH转变成H2时,反应放热,A错误;反应物的总能量小于生成物的总能量时,反应吸热,B错误;液态甲醇转变成气态甲醇时,要吸收热量,液态甲醇参与反应时,放出的热量比气态甲醇的少,ΔH变大,C正确;反应②放热,1 mol CH3OH(g)和![]() mol O2(g)的总能量大于1 mol CO2(g)和2 mol H2(g)的总能量,与图示不符,D错误。
mol O2(g)的总能量大于1 mol CO2(g)和2 mol H2(g)的总能量,与图示不符,D错误。


