题目内容
12.常温下,欲配制密度为1.1g•cm-3、浓度为6mol•L-1的稀盐酸,在体积为100mL、密度为1.19g•cm-3、浓度为12mol•L-1的浓盐酸中需加蒸馏水101mL.分析 设需要在浓盐酸中加VmL水,由于水的密度为1g/mL,故VmL水的质量为Vg,加入水后,所得稀盐酸溶液的质量分数ω%=$\frac{m(溶质)}{m(溶液)}$×100%,列出表达式①.
根据c=$\frac{1000ρω%}{M}$可知:质量分数ω%=$\frac{cM}{1000ρ}$,据此求出所要配制的稀盐酸的质量分数,得出表达式②;
根据①=②即可解得.
解答 解:设需要在浓盐酸中加VmL水,由于水的密度为1g/mL,故VmL水的质量为Vg,加入水后,所得稀盐酸溶液的质量分数ω%=$\frac{m(溶质)}{m(溶液)}$×100%=$\frac{12mol/L×0.1L×36.5g/mol}{1.19g/mL×100mL+Vg}$×100% ①;
根据c=$\frac{1000ρω%}{M}$可知:质量分数ω%=$\frac{cM}{1000ρ}$,即所要配制的稀盐酸的质量分数ω%=$\frac{6mol/L×36.5g/mol}{1000×1.1g/mL}$ ②.
而①②式相等,即$\frac{6mol/L×36.5g/mol}{1000×1.1g/mL}$=$\frac{12mol/L×0.1L×36.5g/mol}{1.19g/mL×100mL+Vg}$×100%
解得V=101mL.
故答案为:101mL.
点评 本题考查了根据溶液的质量分数来进行溶液配制过程中加水体积的求算,难度不大,注重数据的处理是解题关键.

练习册系列答案
相关题目
3.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)⑨的基态原子电子排布式1s22s22p63s23p64s1.
(2)⑦的基态原子电子排布图 .
.
(3)⑩的单质与水反应的化学方程式F2+2H2O=4HF+O2.
(4)表示①与⑦的化合物是由极性(填“极性”、“非极性”)键形成的非极性
(填“极性”、“非极性”)分子.
(5)②的单质的等电子中分子有CO;离子有C22-,它与钙离子形成的化合物与水反应的化学方程式CaC2+2H2O→Ca(OH)2+C2H2↑.
(6)②的氢化物极易溶于水,其中一个原因是它与水之间可形成氢键,写出它的水溶液中所有氢键的表达式N-H…N、O-H…O、N-H…O、O-H…N.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ⑩ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 4 | ⑨ | ⑧ |
(2)⑦的基态原子电子排布图
 .
.(3)⑩的单质与水反应的化学方程式F2+2H2O=4HF+O2.
(4)表示①与⑦的化合物是由极性(填“极性”、“非极性”)键形成的非极性
(填“极性”、“非极性”)分子.
(5)②的单质的等电子中分子有CO;离子有C22-,它与钙离子形成的化合物与水反应的化学方程式CaC2+2H2O→Ca(OH)2+C2H2↑.
(6)②的氢化物极易溶于水,其中一个原因是它与水之间可形成氢键,写出它的水溶液中所有氢键的表达式N-H…N、O-H…O、N-H…O、O-H…N.
20.如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为 .
.
(2)地壳中含量最多的金属元素是Al.写出元素⑥的氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③.④.⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑪与氢氧化钠反应的化学方程式:Si+2NaOH+H2O=Na2SiO3+2H2↑.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.(2)地壳中含量最多的金属元素是Al.写出元素⑥的氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③.④.⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑪与氢氧化钠反应的化学方程式:Si+2NaOH+H2O=Na2SiO3+2H2↑.
7.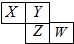 如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的$\frac{7}{10}$,则下列说法中不正确的是( )
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的$\frac{7}{10}$,则下列说法中不正确的是( )
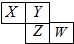 如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的$\frac{7}{10}$,则下列说法中不正确的是( )
如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原子最外层电子数是其内层电子数的$\frac{7}{10}$,则下列说法中不正确的是( )| A. | 原子半径由大到小排列顺序Z>X>Y | |
| B. | Y元素的两种同素异形体在常温下都是气体 | |
| C. | 最高价氧化物对应水化物的酸性W>Z | |
| D. | 阴离子半径由大到小排列顺序X>Y>Z>W |
17.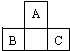 短周期元素A、B、C在元素周期表中的位置如图所示,已知B、C两元素的原子序数之和是A元素原子序数的4倍,A、B、C三元素应分别为( )
短周期元素A、B、C在元素周期表中的位置如图所示,已知B、C两元素的原子序数之和是A元素原子序数的4倍,A、B、C三元素应分别为( )
 短周期元素A、B、C在元素周期表中的位置如图所示,已知B、C两元素的原子序数之和是A元素原子序数的4倍,A、B、C三元素应分别为( )
短周期元素A、B、C在元素周期表中的位置如图所示,已知B、C两元素的原子序数之和是A元素原子序数的4倍,A、B、C三元素应分别为( )| A. | C、Al、P | B. | O、P、Cl | C. | N、Si、S | D. | F、S、Ar |
4.NA表示阿伏加德罗常数的值,下列说法错误的是( )
| A. | 常温常压下46g N02和N204混合气体中含有的原子数为3NA | |
| B. | 由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA | |
| C. | 常温常压下,1mol有机物C2H60中含有极性键的数目一定为7NA | |
| D. | 一定条件下,2mo1 SO2和1mol 02在混合密闭容器中充分反应后,容器中的分子数大于2NA |
19.下列有关说法或化学用语表示正确的是( )
| A. | ${\;}_{6}^{14}C$、${\;}_{7}^{14}N$互为同位素 | |
| B. | NH3的电子式: | |
| C. | 质量数为133、中子数为78的铯原子:${\;}_{78}^{133}Cs$ | |
| D. | ${\;}_{8}^{18}{O}^{2-}$的结构示意图: |
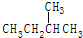
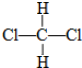 和
和 
