题目内容
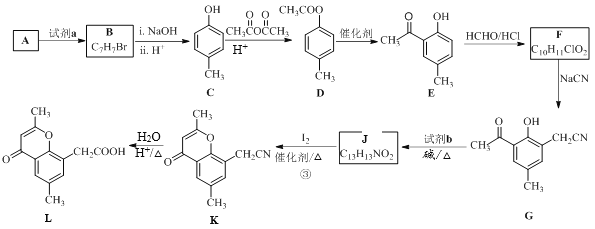
【题目】下图中A~J分别代表相关反应的一种物质。已知A分解得到等物质的量的B、C、D,图中有部分生成物未标出。
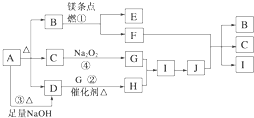
请填写以下空白:
(1)A的化学式________;B的结构式________;D的电子式________;
(2)写出反应①②的化学方程式:
①________________________________________________,
②_________________________________________。
(3)写出反应③的离子方程式:________________________________________。
(4)J与F反应的化学方程式: _________________________________________。
(5)在反应④中,当生成标况下3.36 L G时,转移电子数为__________mol。
【答案】NH4HCO3O=C=O![]() 2Mg+CO2
2Mg+CO2![]() 2MgO+C4NH3+5O2
2MgO+C4NH3+5O2![]() 4NO+6H2ONH4++HCO3-+2OH-
4NO+6H2ONH4++HCO3-+2OH-![]() NH3↑+CO32-+2H2OC+4HNO3(浓)
NH3↑+CO32-+2H2OC+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O0.3
CO2↑+4NO2↑+2H2O0.3
【解析】
A受热能分解,得到等物质的量的B、C、D,且A与碱反应生成D,则A为酸式盐或铵盐,C能和过氧化钠反应,则C为水或二氧化碳,镁条能在B中燃烧,则B为二氧化碳或氧气,因为A受热分解生成B、C、D,则B为二氧化碳,C为水,水和过氧化钠反应生成NaOH和O2,D能在催化剂条件下反应生成H,则D是NH3,G是O2,H是NO,I是NO2,J是 HNO3,镁和二氧化碳反应生成氧化镁和碳,C和浓硝酸反应生成二氧化碳、二氧化氮和水,则E是MgO,F是C,通过以上分析知,A为NH4HCO3;据以上分析解答。
A受热能分解,得到等物质的量的B、C、D,且A与碱反应生成D,则A为酸式盐或铵盐,C能和过氧化钠反应,则C为水或二氧化碳,镁条能在B中燃烧,则B为二氧化碳或氧气,因为A受热分解生成B、C、D,则B为二氧化碳,C为水,水和过氧化钠反应生成NaOH和O2,D能在催化剂条件下反应生成H,则D是NH3,G是O2,H是NO,I是NO2,J是 HNO3,镁和二氧化碳反应生成氧化镁和碳,C和浓硝酸反应生成二氧化碳、二氧化氮和水,则E是MgO,F是C,通过以上分析知,A为NH4HCO3;
(1) 据以上分析可知:A的化学式NH4HCO3;B为二氧化碳,属于共价化合物,结构式O=C=O;D是NH3,属于共价化合物,电子式:![]() ;综上所述,本题答案是:NH4HCO3,O=C=O,
;综上所述,本题答案是:NH4HCO3,O=C=O,![]() 。
。
(2)镁与二氧化碳反应生成氧化镁和碳,反应①的化学方程式:2Mg+CO2![]() 2MgO+C;氨气和氧气发生催化氧化生成一氧化氮和水,反应②的化学方程式:4NH3+5O2
2MgO+C;氨气和氧气发生催化氧化生成一氧化氮和水,反应②的化学方程式:4NH3+5O2![]() 4NO+6H2O ;综上所述,本题答案是:2Mg+CO2
4NO+6H2O ;综上所述,本题答案是:2Mg+CO2![]() 2MgO+C; 4NH3+5O2
2MgO+C; 4NH3+5O2![]() 4NO+6H2O 。
4NO+6H2O 。
(3)碳酸氢铵与过量的氢氧化钠溶液加热反应生成氨气、碳酸钠和水,反应③的离子方程式:NH4++HCO3-+2OH-![]() NH3↑+CO32-+2H2O;综上所述,本题答案是:NH4++HCO3-+2OH-
NH3↑+CO32-+2H2O;综上所述,本题答案是:NH4++HCO3-+2OH-![]() NH3↑+CO32-+2H2O。
NH3↑+CO32-+2H2O。
(4)浓硝酸与碳加热反应生成二氧化碳、二氧化氮和水,反应的化学方程式:C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O;综上所述,本题答案是:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O;综上所述,本题答案是:C+4HNO3(浓) ![]() CO2↑+4NO2↑+2H2O。
CO2↑+4NO2↑+2H2O。
(5)过氧化钠与水反应生成氢氧化钠和氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,反应转移2mole-时,生成氧气1mol,当生成标况下3.36 L 氧气时,即氧气的物质的量为3.36/22.4=0.15mol, 转移电子数为0.3 mol ;综上所述,本题答案是:0.3。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案