题目内容
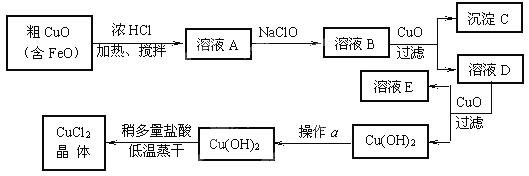
【题目】工业上制取CuCl2的生产流程如下:
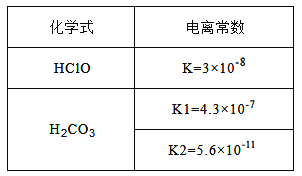
请结合下表数据,回答下列问题:
物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
⑴ 溶液A中加入NaClO的目的是 ;
此反应离子方程式为 ;
⑵ 在溶液B中加入CuO的作用是 ;
⑶ 操作a的目的是 ;
⑷ 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是 。
【答案】⑴ 将Fe2+氧化为Fe3+而使分离更加完全
2 H++ ClO-+2 Fe2+="2" Fe3++Cl-+ H2O

【解析】根据题意,将题中字母所代表的内容填上:A、CuCl2FeCl2; B、 CuC2FeCl3; C、 Fe (OH)3; D 、 CuCl2; E、 NaCl ; a 、洗涤
⑴Fe(OH)3在pH 3~4时沉淀完全,此时Cu2+尚末沉淀,易于分离,故:加入NaClO的目的是将Fe2+氧化为Fe3+而使分离更加完全; 2 H++ ClO-+2 Fe2+="2" Fe3++Cl-+ H2O
⑵调节溶液的pH为3~4,使Fe3+完全转变为Fe (OH)3沉淀而分离Fe3+;
⑶洗涤Cu (OH)2表面的NaCl等可溶性杂质;
⑷Cu2++2H2O![]() Cu(OH)2+2H+,加HCl可抑制Cu2+的水解。
Cu(OH)2+2H+,加HCl可抑制Cu2+的水解。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选用甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,判断滴定终点的现象是__________________。
(2)下列操作中可能使所测NaOH溶液的浓度偏低的是______。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
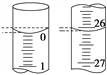
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,所用盐酸溶液的体积为________mL。
(4)某学生根据3次实验分别记录有关数据如下表:
滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.31 | 26.31 |
第二次 | 25.00 | 1.56 | a | 28.74 |
第三次 | 25.00 | 0.22 | 26.51 | b |
表格中a的数值为_________, b的数值为_________。
依据上表数据列式计算该NaOH溶液的物质的量浓度为________________。