题目内容
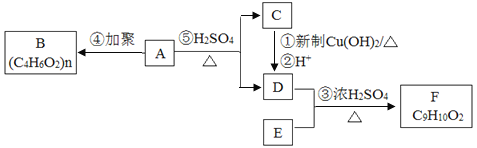
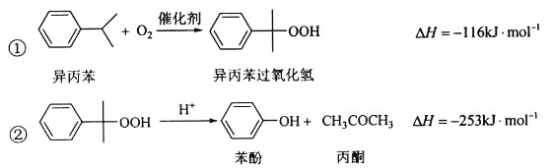
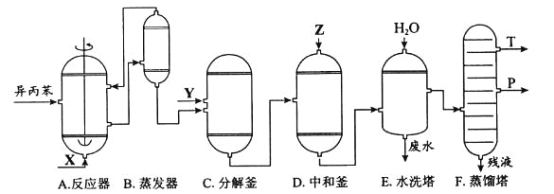
【题目】苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:
相关化合物的物理常数:
物质 | 相对分子质量 | 密度(g/cm-3) | 沸点/℃ |
异丙苯 | 120 | 0.8640 | 153 |
丙酮 | 58 | 0.7898 | 56.5 |
苯酚 | 94 | 1.0722 | 182 |
回答下列问题:
(1)在反应器A中通入的X是_______。
(2)反应①和②分别在装置_______和________中进行(填装置符号)。
(3)在分解釜C中加入的Y为少量浓硫酸,其作用是_____,优点是用量少,缺点是__________。
(4)反应②为_____(填“放热”或“吸热”)反应。反应温度控制在50-60℃,温度过高的安全隐患是_____。
(5)中和釜D中加入的Z最适宜的是__________(填编号)
a.NaOH b.CaCO3c.NaHCO3d.CaO
(6)蒸馏塔F中的馏出物T和P分别为_______和________,判断的依据是______。
(7)用该方法合成苯酚和丙酮的优点是____________。
【答案】氧气(或空气) A C 催化剂(提高反应速率) 腐蚀设备 放热 可能会导致(过氧化物)爆炸 c 丙酮 苯酚 苯酚的沸点高于丙酮 原子利用率高
【解析】
(1)异丙苯被氧气氧化为异丙苯过氧化氢,异丙苯过氧化氢在酸性溶液中分解即可得到苯酚和丙酮,因此在反应器A中通入的X是氧气或空气。
(2)根据流程图可知反应①和②分别在装置A和C中进行。
(3)异丙苯过氧化氢在酸性溶液中分解,所以浓硫酸的作用是作催化剂。由于浓硫酸具有酸性,因此缺点是容易腐蚀设备。
(4)△H小于0,则反应②为放热反应。反应温度控制在50-60℃,由于过氧化物受热易分解,因此温度过高的安全隐患是容易发生爆炸。
(5)苯酚与碳酸氢钠不反应,所以选择碳酸氢钠。
(6)由于苯酚的沸点高于丙酮,丙酮先气化,所以蒸馏塔F中的馏出物T和P分别为丙酮和苯酚。
(7)根据以上分析可知用该方法合成苯酚和丙酮的优点是原子利用率高、没有副产物。

 阶梯计算系列答案
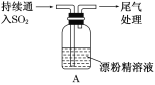
阶梯计算系列答案【题目】某学生对SO2与漂粉精的反应进行实验探究:
操作 | 现象 |
取4g漂粉精固体,加入100mL水 | 部分固体溶解,溶液略有颜色 |
过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
| i.液面上方出现白雾; ii.稍后,出现浑浊,溶液变为黄绿色; iii.稍后,产生大量白色沉淀,黄绿色褪去 |
(1)Cl2和Ca(OH)2制取漂粉精的化学方程式是___。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是___、___。
(3)向水中持续通入SO2,未观察到白雾。推测现象i的白雾由HCl小液滴形成。进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
①实验a的目的是___。
②由实验a、b不能判断白雾中含有HCl,理由是___。
(4)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaCl2溶液,产生白色沉淀。则沉淀X中含有的物质是___。
②用离子方程式解释现象iii中黄绿色褪去的原因:___。
(5)测定漂粉精有效成分的质量分数。称取2.000g漂粉精于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000mol·L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。
反应原理为:3C1O-+I-=3C1-+IO3-,IO3- +5I-+3H2O=6OH-+3I2
实验测得数据如下表所示。
滴定次数 | 1 | 2 | 3 |
KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
该漂白粉中有效成分的质量分数为___。
【题目】“绿水青山就是金山银山”,因此研究NOx、SO2等大气污染物的妥善处理具有重要意义。
(1)燃煤发电厂常利用反应2CaCO3(s)+2SO2(g)+O2(g)=2CaSO4(s)+2CO2(g)△H=-681.8kJ·mol-1对煤进行脱硫处理来减少SO2的排放。对于该反应,在T℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
0 | 10 | 20 | 30 | 40 | 50 | |
O2 | 1.00 | 0.79 | 0.60 | 0.60 | 0.64 | 0.64 |
CO2 | 0 | 0.42 | 0.80 | 0.80 | 0.88 | 0.88 |
0~10min内,平均反应速率υ(O2)__ mol·L-1·min-1;当升高温度,该反应的平衡常数K_____(填“增大”“减小”或“不变”)。
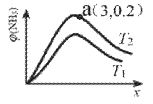
(2)NOx的排放主要来自于汽车尾气,有人利用反应C(s)+2NO(g)![]() N2(g)+CO2(g) △H=-34.0kJ·mol-1,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) △H=-34.0kJ·mol-1,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示:
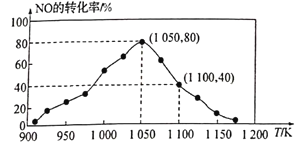
由图可知,1050K前反应中NO的转化率随温度升髙而增大,其原因为__________;在1100K时,CO2的体积分数为_____。
(3)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa时,该反应的化学平衡常数Kp=___ [已知:气体分压(P分)=气体总压(Pa)×体积分数]。
(4)为避免汽车尾气中的有害气体对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=-746.8k·mol-1,生成无毒的N2和CO2。实验测得,υ正=k正·c2(NO)·c2(CO),υ逆=k逆·c(N2)c2(CO2)(k正、k逆为速率常数,只与温度有关)。
N2(g)+2CO2(g) △H=-746.8k·mol-1,生成无毒的N2和CO2。实验测得,υ正=k正·c2(NO)·c2(CO),υ逆=k逆·c(N2)c2(CO2)(k正、k逆为速率常数,只与温度有关)。
①达到平衡后,仅升高温度,k正增大的倍数___(填“>”“<”或“=”)k逆增大的倍数。
②若在1L的密闭容器中充入1 molCO和1 molNO,在一定温度下达到平衡时,CO的转化率为40%,则![]() =_____。
=_____。