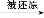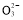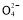题目内容
下列各组离子在指定溶液中一定能大量共存的是( )
A.能使甲基橙呈红色的溶液:Ba2+、Al3+、NO3—、Cl-
B.由水电离出的c(H+)=1×10-11 mol·L-1的溶液:Na+、Mg2+、Cl-、NO3—
C.0.2 mol·L-1的NaNO3溶液:H+、Fe2+、SO42—、Cl-
D.与Fe反应生成H2的溶液:NH4+、K+、SO42—、CO32—
A
【解析】使甲基橙呈红色的溶液显酸性,各离子均能共存,A正确;由水电离出的c(H+)=1×10-11mol·L-1的溶液可能呈酸性也可能呈碱性,Mg2+在碱性条件下不能共存,B错误;NO3—、H+和Fe2+在溶液中发生氧化还原反应,C错误;酸性溶液与Fe反应生成H2,溶液中CO32—与H+不能共存,D错误。

通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)。
SiC Si;SiCl4 SiO2。
(2)如图立方体中心的“”表示硅晶体中的一个原子,请在立方体的顶点用“”表示出与之紧邻的硅原子。

(3)工业上用高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)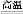 Si(s)+4HCl(g),该反应的反应热ΔH= kJ/mol。
Si(s)+4HCl(g),该反应的反应热ΔH= kJ/mol。
某混合溶液中可能含有的离子如下表所示:
可能大量含有的阳离子 | H+、Ag+、Mg2+、Al3+、NH4+、Fe3+ |
可能大量含有的阴离子 | Cl-、Br-、I-、CO32—、AlO2— |
为探究其成分,进行了以下探究实验。
(1)探究一:
甲同学取一定量的混合溶液,向其中逐滴加入氢氧化钠溶液,产生沉淀的物质的量(n)与加入氢氧化钠溶液的体积(V)的关系如图所示。
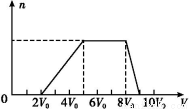
①该溶液中一定不存在的阳离子是 ,
一定不存在的阴离子是 ;含有的阳离子其对应物质的量浓度之比为 ;
②请写出沉淀减少过程中发生反应的离子方程式 。
(2)探究二:
乙同学检测到该溶液中含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,分析后回答下列问题:
Cl2的体积(标准状况) | 11.2 L | 22.4 L | 28.0 L |
n(Cl-) | 2.5 mol | 3.5 mol | 4.0 mol |
n(Br-) | 3.0 mol | 2.5 mol | 2.0 mol |
n(I-) | x mol | 0 | 0 |
①当起始至通入Cl2的体积为22.4 L时,溶液中发生反应总的离子方程式为 ;
②原溶液中Cl-、Br-、I-的物质的量浓度之比为 。