题目内容
在某一化学反应A + 2B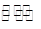 3C中,生成物B的浓度在10s内从1.5 mol/L变成2.0mol/L,则这10s内用生成物C的浓度变化表示的化学反应速率为
3C中,生成物B的浓度在10s内从1.5 mol/L变成2.0mol/L,则这10s内用生成物C的浓度变化表示的化学反应速率为
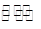 3C中,生成物B的浓度在10s内从1.5 mol/L变成2.0mol/L,则这10s内用生成物C的浓度变化表示的化学反应速率为
3C中,生成物B的浓度在10s内从1.5 mol/L变成2.0mol/L,则这10s内用生成物C的浓度变化表示的化学反应速率为 | A.0.05mol/(L·s) | B.0.05mol/L |
| C.0. 033 mol/(L·s) | D.0. 075 mol/(L·s) |
D
试题分析:生成物B的浓度在10s内从1.5 mol/L变成2.0mol/L,则B物质的浓度变化量是0.5mol/L,所以根据方程式可知,C物质的浓度变化量是0.75mol/L,则10s内用生成物C的浓度变化表示的化学反应速率为0.75mol/L÷10s=0.075 mol/(L·s),答案选D。
点评:该题是基础性试题的考查,主要是考查学生对反应速率含义以及计算的了解掌握情况。另外该题也可以借助于反应速率之比是相应的化学计量数之比进行换算,有利于培养学生的逻辑推理能力和规范答题能力。

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
 2C(g),若经 2 s(秒)后测得C 的浓度为 0.6 mol·L-1 ,则:① 用物质 A 表示的反应的平均速率 ② 2 s 时物质 B 的浓度为 。
2C(g),若经 2 s(秒)后测得C 的浓度为 0.6 mol·L-1 ,则:① 用物质 A 表示的反应的平均速率 ② 2 s 时物质 B 的浓度为 。 2NH3反应中,自反应开始至2S末,氮气的浓度由0变为0.4mol/L,则以氮气的浓度变化表示该反应在2S内的平均反应速率是( )
2NH3反应中,自反应开始至2S末,氮气的浓度由0变为0.4mol/L,则以氮气的浓度变化表示该反应在2S内的平均反应速率是( )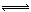 2C(g)+2D(g),在不同条件下的反应速率分别为:
2C(g)+2D(g),在不同条件下的反应速率分别为: 4NO2(g)+ O2(g)。
4NO2(g)+ O2(g)。