题目内容
(6分)把0.04 mol X气体和0.06 mol Y气体混合于2 L密闭容器中,使它们发生如下反应:4X(g)+5Y(g)===nZ(g)+6W(g);2 min末生成0.03 mol W。若测知以Z的浓度变化表示的反应速率为0.005 mol·(L·min)-1。试计算:
(1)前2 min内用X的浓度变化表示的平均反应速率为 ;
(2)化学方程式中n的值是 。
0.005 mol/(L·min); 4
解析试题分析:(1)因为在2 min末生成0.03 mol W,则根据方程式中X与M的物质的量的比为4:6,所以消耗的X的物质的量为0.02mol。因此前2 min内用X的浓度变化表示的平均反应速率为(0.02mol÷2 L)÷2min=0.005 mol/(L·min)。(2)V(Z)=0.005 mol·(L·min)-1,所以在前2分钟内Z的物质的量变化:0.005 mol·(L·min)-1×2min×2L=0.02mol.因为在化学方程式中,物质的方程式前边的系数比等于其物质的量的比,所以n:6="0.02mol:" 0.03 mol。解得n=4。
考点:考查化学反应速率的计算及不同物质间的速率关系的知识。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案(9分) 在一定体积的密闭容器中,进行如下可逆化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K= ;
(2)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
A.容器中压强不变 B.混合气体中 c(CO)不变
C.V正(H2O)= V逆(H2O) D.c(CO2)= c(CO)
(3) 800℃时,反应CO(g)+H2O(g)
 CO2(g)+H2(g)的平衡常数K= 。
CO2(g)+H2(g)的平衡常数K= 。 (16分)化工工业中常用乙苯脱氢的方法制备苯乙烯。
(1)已知某温度下:
反应①:CO2(g) +H2 (g)→CO(g) + H2O(g),ΔH= +41.2 kJ/mol
反应②: 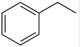 (g)→
(g)→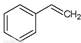 (g)+H2(g),ΔH=" +117.6" kJ/mol
(g)+H2(g),ΔH=" +117.6" kJ/mol
②的化学反应平衡常数分别为K1、K2。
请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式 。该反应的化学平衡常数K= (用K1、K2表示)。
(2)对于反应①,恒温恒容条件下,向密闭容器中加入2molCO2和2molH2,当反应达到平衡后,以下说法正确的是 。
| A.因为该反应是吸热反应,所以升高温度,正反应速率增大,逆反应速率减小; |
| B.若继续加入1molCO2、1mol H2,平衡向正反应方向移动; |
| C.若继续通入1mol CO2则平衡向正反应方向移动,CO2的转化率增大; |
| D.压缩体积,平衡不移动,反应物和产物的浓度都不变; |
(4)已知某温度下, Ag2SO4(M=312g/mol)的溶解度为0.624g/100g H2O,该温度下Ksp(Ag2SO4)= ;(两位有效数字)
(5)电解法制备高铁酸钠(Na2FeO4),总反应式为:Fe+2H2O+2OH- = FeO42-+3H2,电解质溶液选用NaOH溶液。该电解池阳极材料是 (写化学式) ;阳极的电极反应式为: 。
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。汽车尾气中CO与H2O(g)在一定条件下可以发生反应:
CO(g)+H2O(g) CO2(g)+H2(g)ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
CO2(g)+H2(g)ΔH<0。820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
(1)该反应的平衡常数表达式为 。
(2)平衡时,甲容器中CO的转化率是 。比较下列容器中CO的转化率:乙 甲;丙 甲(填“>”、“=”或“<”)。
(3)丙容器中,若要通过改变温度,使CO的平衡转化率增大,则温度需要降低才能达到,则降温后的平衡常数K (填“增大”、“减小”或“不变”)。
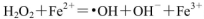
 ,则Fe2+在此过程中所起的作用是______________,当生成336mL O2(标准状况)时,反应中转移电子的物质的量为_______mol。
,则Fe2+在此过程中所起的作用是______________,当生成336mL O2(标准状况)时,反应中转移电子的物质的量为_______mol。


 .
. 2NH3,2 min后测得容器中生成了1mol NH3,试求:
2NH3,2 min后测得容器中生成了1mol NH3,试求:
 CO(g) + H2O(g),
CO(g) + H2O(g), N2O4(g)(正反应为放热反应)。现将一定
N2O4(g)(正反应为放热反应)。现将一定