题目内容
 短周期元素A、B、C、D、E、F原子序数依次增大,A与C可形成A2C2和A2C两种化合物;B的最高价氧化物对应的水化物甲与气体BA3化合生成离子化合物乙;D与A位于同一主族:E与C形成的化合物是大气污染物,容易形成酸雨;F元素最高化合价与最低化合价的代数和为6.
短周期元素A、B、C、D、E、F原子序数依次增大,A与C可形成A2C2和A2C两种化合物;B的最高价氧化物对应的水化物甲与气体BA3化合生成离子化合物乙;D与A位于同一主族:E与C形成的化合物是大气污染物,容易形成酸雨;F元素最高化合价与最低化合价的代数和为6.(1)E在元素周期表中的位置是
第三周期第ⅥA族
第三周期第ⅥA族
(2)由A、C、F三种元素按原子个数比、1:1:1组成的化合物与BA3反应生成B的单质,写出该反应的化学方程式
3HClO+2NH3=3HCl+N2+3H2O
3HClO+2NH3=3HCl+N2+3H2O
.(3)常温下,若甲、乙两溶液的pH均等于5,则由水电离出的
| c(H+)甲 | c(H+)乙 |
10-4
10-4
;乙溶液中所含离子的物质的量浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-)
c(NO3-)>c(NH4+)>c(H+)>c(OH-)
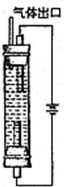
.(4)用如图所示装置电解由D与F形成盐的饱和溶液时,若阴、阳极都用铁作电极,则阳极的电极反应式为
Fe-2e-=Fe2+
Fe-2e-=Fe2+
,溶液中出现的现象是产生气泡,有白色沉淀生成
产生气泡,有白色沉淀生成
.分析:短周期元素A、B、C、D、E、F原子序数依次增大.E与C形成的化合物是大气污染物,容易形成酸雨,E为硫元素、C为氧元素;F元素最高化合价与最低化合价的代数和为6,F处于ⅦA族,则F为Cl元素;A与C可形成A2C2和A2C两种化合物,A处于ⅠA族,D与A位于同一主族,D的原子序数等于氧元素,故A为元素、D为Na元素、A2C2为H2O2、A2C为H2O;B的最高价氧化物对应的水化物甲与气体BH3化合生成离子化合物乙,B为氮元素、甲为硝酸、乙为硝酸铵、BH3为NH3,据此解答.
解答:解:短周期元素A、B、C、D、E、F原子序数依次增大.E与C形成的化合物是大气污染物,容易形成酸雨,E为硫元素、C为氧元素;F元素最高化合价与最低化合价的代数和为6,F处于ⅦA族,则F为Cl元素;A与C可形成A2C2和A2C两种化合物,A处于ⅠA族,D与A位于同一主族,D的原子序数等于氧元素,故A为元素、D为Na元素、A2C2为H2O2、A2C为H2O;B的最高价氧化物对应的水化物甲与气体BH3化合生成离子化合物乙,B为氮元素、甲为硝酸、乙为硝酸铵、BH3为NH3,
(1)E为硫元素,原子核外有3个电子层,最外层电子数为6,处于周期表中第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(2)由H、O、Cl三种元素按原子个数比1:1:1组成的化合物为HClO,与NH3反应生成氮气,根据电子守恒守恒有HCl生成,同时还生成水,反应方程式为3HClO+2NH3=3HCl+N2+3H2O,故答案为:3HClO+2NH3=3HCl+N2+3H2O;
(3)常温下,硝酸溶液中水电离的氢离子等于溶液中氢氧根的浓度为
mol/L=10-9mol/L,硝酸铵溶液中氢离子为水电离产生,浓度为10-5mol/L,故由水电离出的
=
=10-4;
硝酸铵溶液中,铵根离子水解,溶液呈酸性,故溶液中所含离子的物质的量浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-),
故答案为:10-4;c(NO3-)>c(NH4+)>c(H+)>c(OH-);
(4)用如图所示装置电解由NaCl的饱和溶液时,若阴、阳极都用铁作电极,则阳极Fe放电,生成亚铁离子,阳极的电极反应式为 Fe-2e-=Fe2+,阴极氢离子发生生成氢气,溶液中有氢氧氢氧化钠生成,与亚铁离子反应生成氢氧化亚铁沉淀,故现象为:产生气泡,有白色沉淀生成,
故答案为:Fe-2e-=Fe2+;产生气泡,有白色沉淀生.
(1)E为硫元素,原子核外有3个电子层,最外层电子数为6,处于周期表中第三周期第ⅥA族,故答案为:第三周期第ⅥA族;
(2)由H、O、Cl三种元素按原子个数比1:1:1组成的化合物为HClO,与NH3反应生成氮气,根据电子守恒守恒有HCl生成,同时还生成水,反应方程式为3HClO+2NH3=3HCl+N2+3H2O,故答案为:3HClO+2NH3=3HCl+N2+3H2O;
(3)常温下,硝酸溶液中水电离的氢离子等于溶液中氢氧根的浓度为
| 10-14 |
| 10-5 |
| c(H+)甲 |
| c(H+)乙 |
| 10-9mol/L |
| 10-5mol/L |
硝酸铵溶液中,铵根离子水解,溶液呈酸性,故溶液中所含离子的物质的量浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-),
故答案为:10-4;c(NO3-)>c(NH4+)>c(H+)>c(OH-);
(4)用如图所示装置电解由NaCl的饱和溶液时,若阴、阳极都用铁作电极,则阳极Fe放电,生成亚铁离子,阳极的电极反应式为 Fe-2e-=Fe2+,阴极氢离子发生生成氢气,溶液中有氢氧氢氧化钠生成,与亚铁离子反应生成氢氧化亚铁沉淀,故现象为:产生气泡,有白色沉淀生成,
故答案为:Fe-2e-=Fe2+;产生气泡,有白色沉淀生.
点评:本题考查结构性质位置关系、常用化学用语、溶液pH的有关计算、盐类水解、电解原理等,题目较为综合,难度中等,推断元素是解题的关键,(4)中注意活性电极与惰性电极电解的区别.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目