题目内容
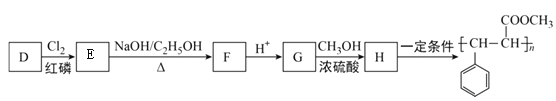
【题目】2.0mol PC13和1.0mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应: PCl3(g)+Cl2(g) ![]() PCl5(g)达平衡时,PCl5为0.40mol,如果此时移走1.0mol PCl3和0.5mol Cl2,在相同温度下再达平衡时PCl3的物质的量是
PCl5(g)达平衡时,PCl5为0.40mol,如果此时移走1.0mol PCl3和0.5mol Cl2,在相同温度下再达平衡时PCl3的物质的量是
A.0.40molB.0.20mol
C.大于0.80mol,小于1.6molD.小于0.80mol
【答案】C
【解析】
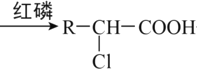
达到平衡后移走1.0mol PCl3和0.5mol Cl2,重新达到平衡,可以等效为开始加入1.0mol PCl3和0.50mol Cl2达到的平衡,与原平衡比压强减小,平衡向逆反应移动,反应物转化率减小,故达到平衡时,PCl3的物质的量大于原平衡的一半,即达到平衡时PCl3的物质的量大于1.6mol×![]() =0.8mol,但小于1.6mol,故选项C正确;
=0.8mol,但小于1.6mol,故选项C正确;
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】某工业流程中,进入反应塔的混合气体中NO和O2的物质的量分数分別为0.10和0.06,发生化学反应2NO(g)+O2(g) ![]() 2NO2(g),在其他条件相同时,测得实验数据如下表:
2NO2(g),在其他条件相同时,测得实验数据如下表:
压强/(×105Pa) | 温度/℃ | NO达到所列转化率需要时间/s | ||
50% | 90% | 98% | ||
1.0 | 30 | 12 | 250 | 2830 |
90 | 25 | 510 | 5760 | |
8.0 | 30 | 0.2 | 3.9 | 36 |
90 | 0.6 | 7.9 | 74 | |
根据表中数据,下列说法正确的是
A.升高温度,反应速率加快
B.增大压强,反应速率变慢
C.在1.0×105 Pa、90℃条件下,当转化率为98%时反应已达平衡
D.若进入反应塔的混合气体为a mol,反应速率以![]() 表示,则在8.0×105Pa、30℃条件下,转化率从50%增至90%时段NO的反应速率为
表示,则在8.0×105Pa、30℃条件下,转化率从50%增至90%时段NO的反应速率为![]() mols-1
mols-1