题目内容
原电池反应通常是放热的氧化还原反应,在理论上可设计成原电池的化学反应是( )A.C(s)+H2O(g)====CO(g)+H2(g);ΔH>0
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)====BaCl2(aq)+2NH3·H2O(l)+8H2O(l);ΔH>0
C.CaC2(s)+2H2O(l)![]() Ca(OH)2(s)+C2H2(g);ΔH<0
Ca(OH)2(s)+C2H2(g);ΔH<0
D.CH4(g)+2O2(g)![]() CO2(g)+2H2O(l);ΔH<0
CO2(g)+2H2O(l);ΔH<0
D
解析:原电池反应是放热的氧化还原反应,放热反应的ΔH<0,所以A、B不合题意;C选项中由于生成物Ca(OH)2微溶于水,会附着在反应物CaC2表面,反应难以继续,并且该反应不是氧化还原反应,C也不合题意。

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
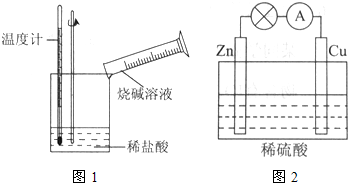 能源是现代社会发展的支柱之一.
能源是现代社会发展的支柱之一.


