题目内容
【题目】钴元素是三元锂离子电池阳极材料的重要成分。请回答下列问题:
(1)钴元素在周期表中的位置是___________,其外围电子排布式为___________。
(2)已知第四电离能大小:I4(Fe)> I4 (Co),从原子结构的角度分析可能的原因是___________。
(3)配位化学创始人维尔纳发现,取1mol配合物CoCl3·6NH3(黄色)溶于水,加人足量硝酸银溶液,产生3mol白色沉淀,沉淀不溶于稀硝酸。原配合物中络离子形状为正八面体。
①根据上述事实推测原配合物中络离子化学式为___________。
②该配合物在热NaOH溶液中发生反应,并释放出气体,该反应的化学方程式___________;生成气体分子的中心原子杂化方式为___________。
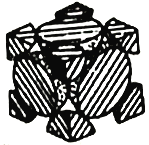
(4)经X射线衍射测定发现,晶体钴在417℃以上堆积方式的剖面图如图所示,则该堆积方式属于___________,若该堆积方式下的晶胞参数为acm,则钴原子的半径为___________pm。
【答案】第四周期VIII族 3d74s2 Fe3+电子排布较稳定的3d5变为不稳定的3d4需要更多的能量 [Co(NH3)6]3+ [Co(NH3)6]Cl3+3NaOH=Co(OH)3↓+6NH3+3NaCl sp3 面心立方堆积 ![]() a
a![]() 1010
1010
【解析】
(1)钴的原子序数为27,在周期表中位于第四周期VIII族,电子排布式为1s22s22p63s23p63d74s2;
(2) Fe3+外围电子排布式为3d5,Co3+外围电子排布式为3d6,由此可知Fe3+从电子排布较稳定的3d5变为不稳定的3d4需要更多的能量;
(3)①1mol配合物CoCl3·6NH3(黄色)溶于水,加人足量硝酸银溶液,产生3mol白色沉淀,沉淀不溶于稀硝酸,说明Cl-是外界离子,不是配位体;络离子形状为正八面体,则说明Co3+与6个NH3形成配位络离子;
②根据以上分析,该配合物为[Co(NH3)6]Cl3,与热NaOH溶液中发生反应,放出气体应为氨气;NH3分子的中心原子的价电子对数为![]() =4,故杂化方式为sp3;
=4,故杂化方式为sp3;
(4)由图可知,该堆积方式属于面心立方堆积;
钴在面心立方堆积中,钴原子处于顶点和面心,设钴原子的半径为r,则晶胞立方体面对角线长为4r,若该堆积方式下的晶胞参数为acm,则(4r)2=a2+a2,解得r=![]() acm=
acm=![]() a
a![]() 1010pm。
1010pm。
(1)钴的原子序数为27,在周期表中位于第四周期VIII族,电子排布式为1s22s22p63s23p63d74s2,其外围电子排布式为3d74s2;
故答案为:第四周期VIII族;3d74s2;
(2) Fe3+外围电子排布式为3d5,Co3+外围电子排布式为3d6,由此可知Fe3+从电子排布较稳定的3d5变为不稳定的3d4需要更多的能量,所以第四电离能大小:I4(Fe)> I4 (Co);
故答案为:Fe3+电子排布较稳定的3d5变为不稳定的3d4需要更多的能量;
(3)①1mol配合物CoCl3·6NH3(黄色)溶于水,加人足量硝酸银溶液,产生3mol白色沉淀,沉淀不溶于稀硝酸,说明Cl-是外界离子,不是配位离子;络离子形状为正八面体,则说明Co3+与6个NH3形成配位络离子。则络离子化学式为[Co(NH3)6]3+;
②根据以上分析,该配合物为[Co(NH3)6]Cl3,与热NaOH溶液中发生反应,放出气体应为氨气,则化学方程式[Co(NH3)6]Cl3+3NaOH=Co(OH)3↓+6NH3+3NaCl;NH3分子的中心原子的价电子对数为![]() =4,故杂化方式为sp3;
=4,故杂化方式为sp3;
故答案为:[Co(NH3)6]3+;[Co(NH3)6]Cl3+3NaOH=Co(OH)3↓+6NH3+3NaCl;sp3;
(4)由图可知,该堆积方式属于面心立方堆积;
钴在面心立方堆积中,钴原子处于顶点和面心,设钴原子的半径为r,则晶胞立方体面对角线长为4r,若该堆积方式下的晶胞参数为acm,则(4r)2=a2+a2,解得r=![]() acm=
acm=![]() a
a![]() 1010pm。
1010pm。
故答案为:面心立方堆积;![]() a
a![]() 1010。
1010。

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案【题目】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
|
|
|
|
A.4.03米大口径碳化硅反射镜 | B.2022年冬奥会聚氨酯速滑服 | C.能屏蔽电磁波的碳包覆银纳米线 | D.“玉兔二号”钛合金筛网轮 |
A. AB. BC. CD. D