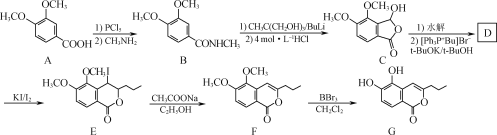
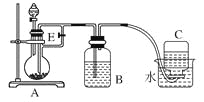
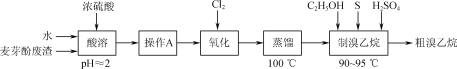
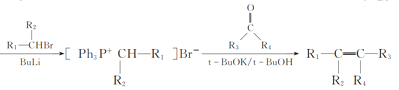题目内容
【题目】铝粉和氧化铁粉末的混合物制成的铝热剂可用于焊接钢轨。现取不同质量的该铝热剂分别和100mL同浓度的NaOH溶液反应,所取铝热剂的质量与产生气体的体积关系如表(气体体积均在标准状况下测定)。
① | ② | ③ | |
铝热剂质量/g | 7.5 | 15.0 | 20.0 |
气体体积/L | 3.36 | 6.72 | 6.72 |
计算:
(1)NaOH溶液物质的量浓度_______
(2)该铝热剂中铝的质量分数_______
(3)15g该铝热剂发生铝热反应理论上产生铁的质量。_______
【答案】NaOH溶液物质的量浓度为2mol·L-1 该铝热剂中铝的质量分数为36% 15g该铝热剂发生铝热反应理论上产生铁的质量为6.72g
【解析】
铝热剂加入NaOH溶液中发生:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
(1)由②③组数据可知NaOH完全反应,根据氢气的体积可计算NaOH溶液物质的量浓度;
(2)根据①组数据计算,①中NaOH剩余,Al完全反应根据化学方程式可计算Al的质量,进而可计算质量分数;
(3)根据(2)Al的质量分数可计算生成铁的质量.
(1)铝热剂加入NaOH溶液中发生:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由②③组数据可知NaOH完全反应,n(H2)=![]() =0.3mol,
=0.3mol,
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2mol 3mol
n(NaOH) 0.3mol
n(NaOH)=0.2mol,
c(NaOH)=![]() =2mol·L-1,
=2mol·L-1,
答:NaOH溶液物质的量浓度为2mol·L-1;
(2)①中NaOH剩余,Al完全反应,n(H2)=![]() =0.15mol,
=0.15mol,
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2mol 3mol
n(Al) 0.15mol
n(Al)=0.1mol,m(Al)=0.1mol×27g·mol-1=2.7g,ω(Al)=![]() ×100%=36%,
×100%=36%,
答:该铝热剂中铝的质量分数为36%;
(3)15 g铝热剂中含n(Al)=![]() =0.2 mol,m(Al)=15g×36%=5.4g,m(Fe2O3)=15g-5.4g=9.6g,n(Fe2O3)=
=0.2 mol,m(Al)=15g×36%=5.4g,m(Fe2O3)=15g-5.4g=9.6g,n(Fe2O3)=![]() =0.06mol,则Al过量,
=0.06mol,则Al过量,
Fe2O3+2Al![]() 2Fe+Al2O3,
2Fe+Al2O3,
1mol 2mol
0.06 mol n(Fe)
n(Fe)=0.12mol
m(Fe)=0.12mol×56g·mol-1=6.72g,
答:15 g该铝热剂发生铝热反应理论上产生铁的质量为6.72 g。