题目内容
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:
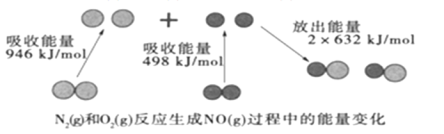
下列说法中正确的是( )
A.1molN2(g)和1molO2(g)完全反应放出的能量为180kJ
B.通常情况下,N2(g)和O2(g)混合能直接生成NO
C.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
【答案】C
【解析】
A.焓变=反应物断裂化学键吸收的能量生成物形成化学键放出的能量,N2+O2═2NO,△H=946kJ/mol+498kJ/mol2×632kJ/mol=+180kJ/mol,反应是吸热反应,故A错误;
B. 通常情况下,N2(g)和O2(g)混合不能直接生成NO,需要放电条件,故B错误;
C. 由图中数据可得反应物键的断裂吸收(946+498)=1444kJ/mol的能量,生成物键的形成放出2×632=1264kJ/mol的能量,故该反应是吸热反应,依据能量守恒,1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量,故C正确;
D. 一氧化氮不是酸性氧化物,物质分类中属于不成盐氧化物,不能和氢氧化钠反应,故D错误;
答案选C。

【题目】含氯化合物在工农业生产和日常生活中有着广泛的用途。
(1)工业上用氯气制备漂白粉,某研究小组利用下列装置制备漂白粉。

①漂白粉的有效成分是_____________(填化学式)。漂白粉放置在空气中一段时间后会失效,原因是(写出有关反应的化学方程式)________________________。
②装置A中发生反应的化学方程式为___________________________________。
③装置B中试剂a为_________,作用是________________________________。
(2)ClO2常用于自来水的消毒、木质纸浆的漂白。已知:NaCl+3H2O![]() NaClO3+3H2↑,2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。有关物质的熔、沸点如下表:
NaClO3+3H2↑,2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。有关物质的熔、沸点如下表:
物质 | 熔点/℃ | 沸点/℃ |
ClO2 | -59 | 11 |
Cl2 | -107 | -34.6 |
ClO2的生产流程示意图如下:

理论上每生成1molClO2,外界至少补充X气体________ mol。从ClO2发生器中分离出ClO2可采用的方法是____________。
【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:![]()
![]() 。相关条件和数据见下表:
。相关条件和数据见下表:
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是( )
A. 实验Ⅲ达平衡后,恒温下再向容器中通入1molA和1molD,平衡不移动
B. 升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C. 实验Ⅲ达平衡后容器内的压强是实验Ⅰ的0.9倍
D. K3>K2>K1