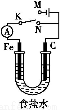
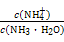题目内容
已知H2A在水中存在以下平衡:H2A H++HA-,HA-
H++HA-,HA- H++A2-。回答以下问题:
H++A2-。回答以下问题:
(1)NaHA溶液 (填“显酸性”、“显碱性”、“显中性”或“酸碱性无法确定”)。
(2)某温度下,若向0.1 mol/L的NaHA溶液中滴入0.1 mol/L KOH溶液使混合溶液中c(H+)=c(OH-),则此时该混合溶液中,下列关系一定正确的是 (填字母)。
A.c(H+)·c(OH-)=1×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05 mol/L
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s) Ca2+(aq)+A2-(aq) ΔH>0
Ca2+(aq)+A2-(aq) ΔH>0
①温度升高时,Ksp (填“增大”、“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+) 。
(4)若向CaA悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式: 。
(1)酸碱性无法确定 (2)B、C (3)①增大 ②增大
(4)CaA(s)+Cu2+(aq) Ca2+(aq)+CuA(s)
Ca2+(aq)+CuA(s)
【解析】(1)HA-是弱酸的酸式酸根离子,既水解又电离,所以酸碱性无法确定。
(2)温度不确定,所以KW不确定,c(H+)·c(OH-)不一定等于1×10-14,A错;B项遵循电荷守恒,正确;因为加入KOH溶液使混合溶液中c(H+)=c(OH-),可知NaHA溶液显弱酸性,所以当溶液显中性时,滴入的KOH溶液的量小于NaHA溶液的量,故c(Na+)>c(K+),C项正确;混合溶液中c(Na+)+c(K+)>0.05 mol/L,D项错误。
(3)Ksp=c(Ca2+)×c(A2-),该过程是吸热过程,升温平衡向右移动,所以Ksp增大;滴加少量浓盐酸,A2-与H+结合,使平衡向右移动,所以c(Ca2+)增大。
(4)沉淀转化为更难溶的沉淀:CaA(s)+Cu2+(aq) Ca2+(aq)+CuA(s)。
Ca2+(aq)+CuA(s)。

 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案一定温度时,向2.0 L恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:
2SO2(g)+O2(g)  2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | t1 | t2 | t3 | t4 |
n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是( )
A.反应在前t1s的平均速率v(O2)=0.4/t1 mol·L-1·s-1
B.保持其他条件不变,体积压缩到1.0 L,平衡常数将增大
C.相同温度下,起始时向容器中充入4 mol SO3,达到平衡时,SO3的转化率大于10%
D.保持温度不变,向该容器中再充入2 mol SO2、1 mol O2,反应达到新平衡时n(SO3)/n(O2)增大
T ℃、2 L密闭容器中某一反应在不同时刻的各物质的量如图所示(E为固体,其余为气体)。回答下列问题。
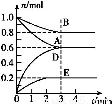
(1)写出该反应的化学方程式: 。
(2)反应开始至3 min时,用D表示的平均反应速率为 mol·L-1·min-1。
(3)T ℃时,该反应的化学平衡常数K= 。
(4)第6 min时,保持温度不变,将容器的体积缩小至原来的一半,重新达到平衡后,D的体积分数为 。
(5)另有一个2 L的密闭容器,T ℃、某一时刻,容器中各物质的物质的量如表所示。
物质 | A | B | D | E |
物质的量(mol) | 0.8 | 1.0 | 0.4 | 0.2 |
此时v(正) v(逆)(填“大于”、“等于”或“小于”)。