��Ŀ����
����Ŀ��������ѧ֪ʶ������ش��������⣺
��1��д��ԭ��������С�ĵڢ���Ԫ��ԭ�ӵ�ԭ�ӽṹʾ��ͼ__________��
��2��д��3p�������2��δ�ɶԵ��ӵ�Ԫ�صķ��ţ�______________��
��3����Ԫ�ر���ѧ�ҳ�֮Ϊ������Ԫ���еġ�����֮��������ԭ�ӵ���Χ�����Ų�ʽΪ4s24p4����Ԫ�ص�������____________��
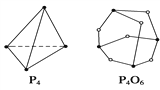
��4����ѧ��Ӧ����Ϊ�ɼ��Ķ��Ѻ��¼����γɹ��̡���ѧ���ļ������γɻ�ѧ��ʱ�ͷŵ���������֪����P4O6�ķ��ӽṹ��ͼ��ʾ�����ṩ���»�ѧ���ļ���(kJ��mol��1)��P��P��198��P��O��360��O===O��498����ӦP4(����)��3O2===P4O6�ķ�Ӧ�Ȧ�HΪ___________________
��5��д�����������ˮ����������Sԭ�ӣ�Oԭ�ӷֱ����______��______�ӻ���ʽ����ռ乹�ͷֱ�Ϊ________��__________��
��6���������ʾ����ʾHFˮ��Һ�е��������__________________��
���𰸡� ![]() Si��S �� ��1 638 kJ��mol��1 sp2 sp 3 V�� ������ F��H��F F��H��O O��H��O O��H��F
Si��S �� ��1 638 kJ��mol��1 sp2 sp 3 V�� ������ F��H��F F��H��O O��H��O O��H��F
��������(1)������Ԫ���������ܡ�����ԭ��������С��������ԭ�Ӻ�����26�����ӣ���ԭ�ӽṹʾ��ͼΪ��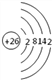 ��(2)3p�������2��δ�ɶԵ���ʱ�����������һ������һ��3p�����û�е��ӣ�һ������һ��3p����ϳ������ӣ����Ե���һ��3p�����û�е��ӣ���ԭ����Si��һ������һ��3p����ϳ������ӣ���ԭ����S��(3)ԭ�ӵ���Χ�����Ų���4s24p4��˵����ԭ���и���������������ӣ���ԭ�Ӻ����������34����������Ԫ�أ�
��(2)3p�������2��δ�ɶԵ���ʱ�����������һ������һ��3p�����û�е��ӣ�һ������һ��3p����ϳ������ӣ����Ե���һ��3p�����û�е��ӣ���ԭ����Si��һ������һ��3p����ϳ������ӣ���ԭ����S��(3)ԭ�ӵ���Χ�����Ų���4s24p4��˵����ԭ���и���������������ӣ���ԭ�Ӻ����������34����������Ԫ�أ�
(4)����ȼ�շų�������=������ļ���-��Ӧ��ļ���=12��360kJ-(6��198)kJ-(3��498)kJ=1638kJ����Ӧ���ʱ���-1638KJ/mol����ӦP4(����)ȼ������P4O6���Ȼ�ѧ����ʽΪ��P4(s)+3O2(g)=P4O6(g)��H=-1638KJ/mol��
(5)�������������Oԭ�Ӽ۲���Ӷ�2+![]() (6-2��2)=3����ԭ�ӹ¶Ե��Ӷ���Ϊ1����ԭ�Ӳ�ȡsp2�ӻ������������������ԭ�Ӽ۲���Ӷ�2+
(6-2��2)=3����ԭ�ӹ¶Ե��Ӷ���Ϊ1����ԭ�Ӳ�ȡsp2�ӻ������������������ԭ�Ӽ۲���Ӷ�2+![]() (6-2��2)=3����ԭ�ӹ¶Ե��Ӷ���Ϊ1���ռ乹��ΪV�Σ�ˮ������������ԭ�ӵļ۲���Ӷ�3+
(6-2��2)=3����ԭ�ӹ¶Ե��Ӷ���Ϊ1���ռ乹��ΪV�Σ�ˮ������������ԭ�ӵļ۲���Ӷ�3+![]() (6-1-3��1)=4����ԭ�ӹ¶Ե��Ӷ���Ϊ1����ԭ�Ӳ�ȡsp3�ӻ���ˮ�������ӿռ乹��Ϊ�����ͣ�(6)N��O��F����ԭ��֮�����γ������F���⻯����Һ��Ϊ������ˮ��Һ������HF�����Լ�H2O���ӣ����ڵ��������ΪF-H��F��F-H��O��O-F��F��O-H��O��
(6-1-3��1)=4����ԭ�ӹ¶Ե��Ӷ���Ϊ1����ԭ�Ӳ�ȡsp3�ӻ���ˮ�������ӿռ乹��Ϊ�����ͣ�(6)N��O��F����ԭ��֮�����γ������F���⻯����Һ��Ϊ������ˮ��Һ������HF�����Լ�H2O���ӣ����ڵ��������ΪF-H��F��F-H��O��O-F��F��O-H��O��

����Ŀ����ˮ�Ǿ����Դ���⡣��ͼ��ʵ����ģ�ҵ�Ӻ�ˮ��Դ��ȡijЩ��Ҫ����ԭ�ϵ�����ʾ��ͼ��
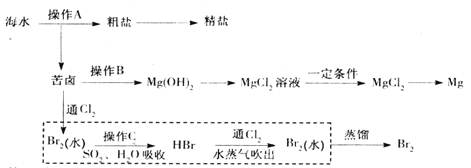
�ش��������⣺
(1)�����������ں�ˮ��Ũ�Ⱥܵͣ�0.067g/L����Ҫ������Ԫ�ص�Ũ����������ʵ������Ҫֱ��Ũ����ˮʱ������������϶�����Ҫ���ǣ����ţ�__________
A�������� B�����ż� C������ D�������� E���ƾ���
(2)Ҫ֪����ˮɹ�εĹ�������Һ��ʳ�κ���������ߵļ�������___________��
A�������Ȼ��ƺ��� B���ⶨ��Һ�ܶ� C���۲��Ƿ��г�������
(3)д����ˮ��ͨ��SO2ʱ��Ӧ�����ӷ���ʽ____________��
(4)��ͼ�����߿�������Ҳ����![]() Na2CO3��Һ����Br2�ķ�Ӧ��ѧ����ʽ����������
Na2CO3��Һ����Br2�ķ�Ӧ��ѧ����ʽ����������
____Br2 + _____Na2CO3 = _____NaBrO3 +___________ +________
(5)����һ�������������ɫ��Һ(�����������ַ���֮һ�������ռ�����ǡ����ȫ��Ӧ)������ͨ��ʵ��̽������Һ�����Dz������ַ���������ġ�
�� �����������
����1�����ô������շ�������Һ�к�����Na+��Br �C��BrO3-
����2��_____________________________________________��
�� ��Ʒ���������ʵ�飬��֤���裺���ڱ���д��ʵ�鲽���Լ�Ԥ������ͽ��ۡ���ѡʵ���Լ���������10mL��Ͳ��С�ձ����Թܡ���ͷ�ιܣ���ˮ�Ҵ�������0.10mol/LAgNO3��0.10mol/LBaCl2��2mol/LHCl �����ϵã�Ba(BrO3)2Ϊ��ɫ���壬����ˮ
ʵ�鲽�� | Ԥ������ͽ��� |
����1������Ͳȡ��Ʒ��Һ2mL�ֱ���A��B�Թ���,��A�Թ��м���___________�� | ��____________________________�������1һ���ܳ����� |
����2�����Թ�B�м���___________�� | ��_________________�������2һ���ܳ����� |