��Ŀ����
����Ŀ��D��E��X��Y��Z�����ڱ��е�ǰ20��Ԫ�أ���ԭ��������������ǵ�����⻯����ӵĿռ�ṹ�������������塢�����Ρ�ֱ���Ρ������Ρ�ֱ���Σ��ش��������⣺
��1��E���⻯��ĵ���ʽΪ_____��D���⻯������м���Ϊ_____��Y���⻯��ĽṹʽΪ_____��X���⻯��е�_____Z���⻯��е㣨����ڡ����ڡ�����
��2��D��Y�γɵĻ��������ӵĵ���ʽΪ_____���ռ乹��Ϊ_____�Σ�Ϊ_____������ԡ��Ǽ��ԡ������ӡ�
��3��ȡ���������⻯���е����ֻ��ϣ�������һ�ֺ������Ӽ������ۼ�����λ���Ļ������д�����е�����һ�ֵĻ�ѧʽ_____��
���𰸡�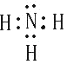 109��28�� H��S��H ����
109��28�� H��S��H ���� ![]() ֱ���� �Ǽ��� NH4Cl
ֱ���� �Ǽ��� NH4Cl
��������
D��E��X��Y��Z�Ƕ�����Ԫ�أ���ԭ���������������ǵ�����⻯����ӵĿռ�ṹ�������������塢�����Ρ�ֱ���Ρ������Ρ�ֱ���Σ��γ���������ṹ���⻯����CH4��SiH4���γ������͵��⻯����NH3��PH3���γ������ε��⻯����H2O��H2S���γ�ֱ���ͽṹ���⻯����HCl��HF���⼸��Ԫ�ص�ԭ����������������D���⻯����CH4��E���⻯����NH3��X���⻯����HF��Y���⻯����H2S��Z���⻯����HCl����D��E��X��Y��Z�ֱ���C��N��F��S��ClԪ�أ��Դ˽����⡣
D��E��X��Y��Z�Ƕ�����Ԫ�أ���ԭ���������������ǵ�����⻯����ӵĿռ�ṹ�������������塢�����Ρ�ֱ���Ρ������Ρ�ֱ���Σ��γ���������ṹ���⻯����CH4��SiH4���γ������͵��⻯����NH3��PH3���γ������ε��⻯����H2O��H2S���γ�ֱ���ͽṹ���⻯����HCl��HF���⼸��Ԫ�ص�ԭ����������������D���⻯����CH4��E���⻯����NH3��X���⻯����HF��Y���⻯����H2S��Z���⻯����HCl����D��E��X��Y��Z�ֱ���C��N��F��S��ClԪ�أ�
��1��E���⻯����NH3�������ĵ���ʽΪ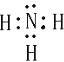 ��D���⻯����CH4������Ϊ109��28�䣬Y���⻯����H2S���ṹʽΪH��S��H��HF���Ӽ����������е�ϸߣ�
��D���⻯����CH4������Ϊ109��28�䣬Y���⻯����H2S���ṹʽΪH��S��H��HF���Ӽ����������е�ϸߣ�
�ʴ�Ϊ��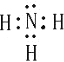 ��109��28�䣻H��S��H�����ڣ�
��109��28�䣻H��S��H�����ڣ�
��2��D��Y�γɵĻ�����ΪCS2������ʽΪ![]() ��Ϊֱ���η��ӣ��ṹ�Գƣ�Ϊ�Ǽ��Է��ӣ�
��Ϊֱ���η��ӣ��ṹ�Գƣ�Ϊ�Ǽ��Է��ӣ�
�ʴ�Ϊ��![]() ��ֱ���Σ��Ǽ��ԣ�
��ֱ���Σ��Ǽ��ԣ�
��3�����������⻯���е����ֻ��ϣ�������һ�ֺ������Ӽ������ۼ�����λ���Ļ������Ϊ��Σ���ΪNH4Cl�ȣ�
�ʴ�Ϊ��NH4Cl��

 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�����Ŀ�����ܼ��Ŵ�ʩ���ҹ���ʮһ�����ڼ���������ߴ�ʩ��
(1)ú��ȼ�գ�����������к����塣��úת��Ϊˮú��������Ч�����ŷš�
C(s)+O2(g)=CO2(g) ��H=��393.5 kJ��mol��1
H2(g)+ ![]() O2(g)=H2O(g) ��H=��242.0kJ��mol��1
O2(g)=H2O(g) ��H=��242.0kJ��mol��1
CO(g)+![]() O2(g)=CO2(g) ��H=��283.0kJ��mol��1
O2(g)=CO2(g) ��H=��283.0kJ��mol��1
�����������ݣ�д��C(s)��ˮ������Ӧ����CO��H2���Ȼ�ѧ����ʽ___________��
(2)����β�����ŷ��Ǵ�����Ⱦ�����Ҫ��Դ�����к���NO���塣����������ʾ�û���̿��ԭ�����Դ����������ij�x��С����̶��ݻ����ܱ������м���һ�����Ļ���̿��NO������ӦC(s)+2NO(g)![]() CO2(g)+N2(g) ��H=��574kJ��mol��1�������¶�Tʱ�����ⷴӦ�����Ƴ��±���
CO2(g)+N2(g) ��H=��574kJ��mol��1�������¶�Tʱ�����ⷴӦ�����Ƴ��±���

��0��10min�ڣ�NO��ƽ����Ӧ����v(NO)=___________mol��L��1��min��1��
���������ݲ��ٱ仯�ɱ�ʾ�÷�Ӧ�ﵽƽ�����___________��
a.������ѹǿ b����������ƽ��Ħ������ c�����������ܶ�
����������Ϊ�ɱ��ݻ���������ƽ���ı�ijһ������һ��ʱ���Ӧ�ٴδﵽԭƽ�⣬��д�����ܸı��������___________(��дһ��)��
(3)��ij�¶�Tʱ��ͬʱ������Ӧ��
2N2O5(g)![]() 2N2O4(g)+O2(g) K1
2N2O4(g)+O2(g) K1
N2O4(g)![]() 2NO2(g) K2
2NO2(g) K2
����һ����̶�Ϊ2L���ܱ������ڼ���N2O52mol��һ��ʱ��������ڵķ�Ӧ�ﵽƽ�⣬��ʱn(NO2)=0.4mol����֪K2=0.1��������K1=___________��
(4)һ�������£�������β��ͨ�뵽����������Һ��β���е������������ת��Ϊ�������ƣ���ҵ�Ͽ����������������Ʊ������ᡣ��֪��25��ʱ������(HNO2)��������(H2SO3)�ĵ���ƽ�ⳣ���ֱ����£�
Ka1 | Ka2 | |
�����ᣨHNO2�� | 7.1��10-4 | |
�����ᣨH2SO3�� | 1.54��10-2 | 1.02��10-7 |
��ش���������
�������£���0.1mol��L��1��������ϡ��100����c(H+)��___________(������������������������С��)��Kaֵ��(��������������������������С��)___________��
���������ӷ���ʽ�ܷ�������___________(����ĸ)��
a��NO2��+SO2+H2O=HNO2 +HSO3�� b�� 2HNO2+SO32��=2NO2��+SO2��+H2O
c��2NO2��+SO2 +H2O=2HNO2 +SO32�� d�� HNO2+SO32��= NO2��+ HSO3��
����Ŀ��I����һ��������aA��bB![]() cC+dD�ﵽƽ��ʱ������д��
cC+dD�ﵽƽ��ʱ������д��
��1����A��B��C��D�������壬�ڼ�ѹ��ƽ�����淴Ӧ�����ƶ�����a��b��c��d��ϵ��__________________��
��2����֪B��C��D�����壬������A�����ʵ�����ƽ�ⲻ�ƶ���˵��A��__________________����״̬����
��3���������ݻ����䣬��������B������A��ת����__________________����������������С����������������
��4�������Ⱥ�C�İٷֺ�����С��������Ӧ��__________________��Ӧ��������������������������
��5������������ѹǿ���䣬��A��B��C��D�������壬�������г���ϡ�����壬��ѧƽ�������ƶ�����a��b��c��d��ϵ��__________________��
������ҵ��һ��������з�Ӧ�ϳɼ״���CO(g)��2H2(g) ![]() CH3OH(g)��
CH3OH(g)��
��1����һ���¶��£���2 mol CO��6 mol H2����2 L���ܱ������У���ַ�Ӧ�ﵽƽ��ʱ���c(CO)��0.5mol��L��1���÷�Ӧ��ƽ�ⳣ��K��__________________��
��2������һ����ɱ�������г���l molCO�� 2mol H2��1mol CH3OH���ﵽƽ�ⅼ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6������÷�Ӧ��__________________(����������������)��Ӧ�����ƶ���
��3�������¶Ⱥ��ݻ���ͬ�������ܱ������У�����ͬ��ʽͶ�˷�Ӧ���÷�Ӧ�ﵽƽ�ⅼ���й��������±���
���� | ��Ӧ��Ͷ����� | ��Ӧ���ת���� | CH3OH��Ũ��(mol/L) | �����仯��Q1��Q2��Q3������0�� |
1 | 2molCO��4molH2 | a1�� | c1 | �ų�Q1kJ���� |
2 | 2molCH3OH | a2�� | c2 | ����Q2kJ���� |
3 | 4molCO��8molH2 | a3�� | c3 | �ų�Q3kJ���� |
�����й�ϵ��ȷ���� __________________��
A�� c1=c2 B��2Q1=Q3 C��2a1=a3 D��a1 +a2 =1 E���÷�Ӧ������2mol CH3OH����ų�(Q1+Q2)kJ����




