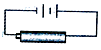题目内容
【题目】如图,利用电解原理将NO转化为NH4NO3,既节约了资源,又保护了环境。下列有关说法正确的是
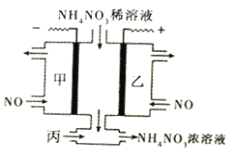
A. NO转化为NH4NO3的反应属于氮的固定
B. 阴极上发生还原反应,电极反应式为:NO+5H++5e-==NH3·H2O
C. 电解池两极上分别生成的甲是NH4+,乙是NO3-
D. 为使电解产物全部转化为NH4NO3,需补充的物质丙为HNO3
【答案】C
【解析】A. NO属于含氮元素的化合物,转化为NH4NO3的反应不属于氮的固定,故A错误;B. 阴极上发生还原反应,根据图像,NO得到电子,化合价降低生成铵根离子,电极反应式为:NO+6H++5e-== NH4++H2O,故B错误;C.根据B的分析,电解池阴极上生成的是NH4+,阳极上NO被氧化生成的是NO3-,故C正确;D. 阳极上NO被氧化生成的是NO3-,阳极反应为NO-5e-+2H2O=NO3-+4H+,阴极上NO得到电子被还原生成铵根离子,阴极反应为:NO+5e-+6H+=NH4++H2O,总反应方程式为:8NO+7H2O![]() 3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3,故D错误;故选C。
3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3,故D错误;故选C。

练习册系列答案
相关题目