��Ŀ����
��800��ʱ�����ݻ�Ϊ2L�ĺ����ܱ������г���һ������CO��H2Oά�ֺ��£�������ӦCO(g)+H2O(g) H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
|
��Ӧʱ��/min |
0 |
2 |
4 |
6 |
|
n(CO)/mol |
1.20 |
0.90 |
|
0.80 |
|
n(H2O)/ mol |
0.60 |
|
0.20 |
|
�ٷ�Ӧ��2 min�ڵ�ƽ������Ϊv(H2O)��___________��
��800��ʱ����ѧƽ�ⳣ��K��ֵΪ_______________��
�۱��������������䣬��ƽ����ϵ����ͨ��0.20 mol H2O����ԭƽ����ȣ��ﵽ��ƽ��ʱCOת����______�������С�����䡱����
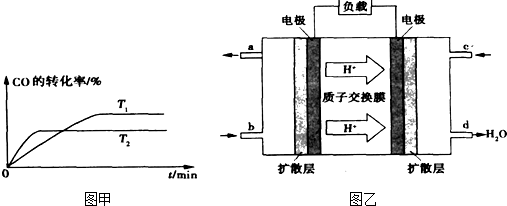
���ں��º�ѹ�ܱ�������ͨ��CO��H2O��1 mol�����÷�Ӧ������Ӧ�ﵽƽ���ά���¶���ѹǿ���䣬t1ʱ��ͨ���1 mol��CO��H2O�Ļ�����壬������ͼ�л�����(v��)����(v��)��Ӧ������t1����ʱ��t�仯������ͼ��

��.ʵ���������ø��ֽⷴӦ��ȡMg(OH)2��ʵ�����ݺ��������±���ʾ����Һ�����ȡ��1mL����
|
��� |
ҩƷ1 |
ҩƷ2 |
ʵ������ |
|
I |
0.01 mol/L NaOH��Һ |
0.01 mol/L MgCl2��Һ |
���ɰ�ɫ���� |
|
II |
0.01 mol/L��ˮ |
0.01 mol/L MgCl2��Һ |
������ |
|
III |
0.1 mol/L��ˮ |
0.1 mol/L MgCl2��Һ |
����III |
|
IV |
0.1 mol/L��ˮ |
0.01 mol/L MgCl2��Һ |
���ɰ�ɫ���� |
|
V |
0.01 mol/L��ˮ |
0.1 mol/L MgCl2��Һ |
������ |
������III�� ��
�������0.028 mol/L��MgCl2��Һ�м���������NaOH��Һ�������NaOH��Һ��Ũ�����ٴﵽ
mol/Lʱ����Һ�п�ʼ���ְ�ɫ������Ksp(Mg(OH)2)= 5.6��10-12����
��MgCl2��Һ�Ͱ�ˮ��Ϻ�������л�ѧƽ�⣺Mg2+(aq)
+ 2NH3��H2O(aq) 2NH4+(aq)
+ Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK=
���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ
��
2NH4+(aq)
+ Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK=
���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ
��
����15�֣��� ��0.075 mol��L��1��min��1��2�֣� ��1��2�֣� ������(1��)
�� ��2�֣�
��2�֣�
�� �����ɰ�ɫ������2�֣� ��4��10-5 mol��L��1��2�֣���K�� ��
��
K��Kb2/Ksp����2�֣�
��������
�����������.�ٸ��ݱ������ݿ�֪����Ӧ��2 minʱCO�����ʵ���������1.20mol��0.90mol��0.30mol�����ݷ���ʽ��֪��ˮ���������ʵ���Ҳ����0.30mol����Ũ����0.30mol��2L��0.15mol/L������2min�ڵ�ƽ������Ϊv(H2O)��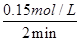 ��0.075 mol��L��1��min��1��
��0.075 mol��L��1��min��1��
��2minʱˮ���������ʵ�����0.30mol��3minʱ��0.20mol������0.10mol����3minʱCO�����ʵ�����0.80mol������4minʱCO�����ʵ���Ҳ��0.8mol����˵����Ӧ��3minʱ�ﵽƽ��״̬����
CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
��ʼŨ�ȣ�mol/L�� 0.60 0.30 0 0
ת��Ũ�ȣ�mol/L�� 0.20 0.20 0.20 0.20
ƽ��Ũ�ȣ�mol/L�� 0.40 0.10 0.20 0.20
����ƽ�ⳣ��K�� ��1.0
��1.0
�۱��������������䣬��ƽ����ϵ����ͨ��0.20 mol H2O������ˮ������Ũ�ȣ�ƽ��������Ӧ������У����CO��ת��������
��ά���¶���ѹǿ���䣬t1ʱ��ͨ���1 mol��CO��H2O�Ļ�����壬���������ݻ���Ȼ�������ڷ�Ӧǰ��������䣬����ƽ���ǵ�Ч�ġ�������Ӧ���������淴Ӧ���ʼ�С����ƽ��״̬���䣬�����ȷ��ͼ���� ��
��
�� �ٸ��ݱ������ݿ�֪��ʵ���͢���ȣ���ˮ��Ũ����ͬ��ʵ������Ȼ�þ��Ũ�ȸ���ʵ������Ȼ�þ��Ũ�ȡ�����ʵ������а�ɫ����������þ���ɣ��������Ԣ���һ�����ɰ�ɫ����������þ��
����NaOH��Һ��Ũ�����ٴﵽx�����������Һ����OH��Ũ��0.5x�����ڻ�Ϻ���Һ��þ����Ũ����0.014mol/L������Ҫ����������þ��������(0.5x)2��0.014��5.6��10-12�����x��4��10-5 mol/L��
�ۻ�ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪���ÿ��淴Ӧ��ƽ�ⳣ��K�� ��K��
��K�� ��Kb2/Ksp��
��Kb2/Ksp��
���㣺���鷴Ӧ���ʺ�ƽ�ⳣ���ļ��㣻���������ƽ��״̬��Ӱ�죻�ܽ�ƽ���Լ��ܶȻ������ļ����Ӧ�õ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�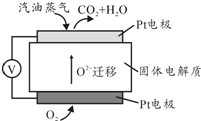 ͨ��ú��������Һ����ʹ̼���仯������Թ㷺Ӧ�ã�
ͨ��ú��������Һ����ʹ̼���仯������Թ㷺Ӧ�ã�I����ҵ������úת��ΪCO��������CO��ˮ������Ӧ��H2ʱ����������ƽ�⣺CO��g��+H2O��g��?CO2��g��+H2��g��
��1����1L�����ܱ������г���CO��H2O��g����800��ʱ��ò����������±���
| t/min | 0 | 1 | 2 | 3 | 4 |
| n��H2O��/mol | 0.600 | 0.520 | 0.450 | 0.350 | 0.350 |
| n��CO��/mol | 0.400 | 0.320 | 0.250 | 0.150 | 0.150 |
��2����ͬ�����£���2L�����ܱ������г���1mol CO��1mol H2O��g����2mol CO2��2mol H2����ʱ�ԣ�����
����֪CO��g����H2��g����CH3OH��l����ȼ���ȷֱ�Ϊ283kJ?mol-1��286kJ?mol-1��726kJ?mol-1��
��3������CO��H2�ϳ�Һ̬�״����Ȼ�ѧ����ʽΪ
��4�����ݻ�ѧ��Ӧԭ������������ѹǿ���Ʊ��״���Ӧ��Ӱ��
��Ϊ���Ѷ�ʯ�͵Ĺ���������������Ա��úҺ���Ʊ����ͣ������������ȼ�ϵ�أ���ع���ԭ����ͼ��ʾ��һ���缫ͨ����������һ�缫ͨ������������������Dz�����Y2O3��ZrO2���壬���ڸ������ܴ���O2-��
��5�������飨C8H18���������ͣ�д���õ�ع���ʱ�ĸ�����Ӧ����ʽ
��6����֪һ�����ӵĵ�����1.602��10-19C���øõ�ص�ⱥ��ʳ��ˮ������·��ͨ��1.929��105C�ĵ���ʱ������NaOH
����úȼ�ղ�����CO2���������ЧӦ����Ҫ����֮һ��
��7����CO2ת�����л������Ч��ʵ��̼ѭ�����磺
a��6CO2+6H2O
| ����/Ҷ���� |
b��2CO2+6H2
| ||
| �� |
c��CO2+CH4
| ||
| �� |
d��2CO2+6H2
| ||
| �� |
���Ϸ�Ӧ�У�����ܵ���
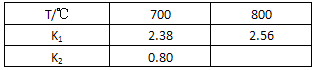
 FeO(s)+H2(g) ��H1 ƽ�ⳣ��ΪK1
FeO(s)+H2(g) ��H1 ƽ�ⳣ��ΪK1  H2(g)+CO2(g) ��H2 ƽ�ⳣ��ΪK2
H2(g)+CO2(g) ��H2 ƽ�ⳣ��ΪK2  FeO(s)+CO(g) ��H3 ƽ�ⳣ��ΪK3
FeO(s)+CO(g) ��H3 ƽ�ⳣ��ΪK3