题目内容
19. 双氰胺结构简式如图.
双氰胺结构简式如图.(1)双氰胺的晶体类型为分子晶体.
(2)双氰胺所含元素中,氮 (填元素名称)元素基态原子核外未成对电子数最多.
(3)双氰胺分子中σ键和π键数目之比为3:1.
分析 (1)由分子构成的晶体是分子晶体;
(2)氮元素基态原子核外未成对电子数最多;
(3)共价单键是σ键,共价双键中一个是σ键一个是π键,共价三键中一个σ键两个π键.
解答 解:(1)根据图象知,双氰胺的构成微粒是分子,所以属于分子晶体,
故答案为:分子晶体;
(2)构成双氰胺的元素中,C元素未成对电子数是2,N元素未成对电子数是3,H元素未成对电子数是1,所以未成对电子数最多的元素是N元素,
故答案为:氮;
(3)共价单键是σ键,共价双键中一个是σ键一个是π键,共价三键中一个σ键两个π键,所以含有σ键与π键个数之比=9:3=3:1,
故答案为:3:1.
点评 本题考查了晶体类型的判断、电子排布、共价键的类型,这些都是高考热点,注意根据结构简式分析,题目难度不大.

练习册系列答案
相关题目
10.下列关于“反应先后顺序”的评价中正确的是( )
| A. | 向CuSO4溶液中滴加氨水,先生成深蓝色溶液,后生成蓝色沉淀 | |
| B. | 向NH4Fe(SO4)2溶液中滴加少量NaOH溶液,NH4+先发生反应 | |
| C. | 向等浓度的FeCl3和CuCl2混合溶液中加入少量Fe粉,Cu2+先被还原 | |
| D. | 足量锌与浓硫酸反应,先产生二氧化硫,后产生氢气 |
7.下列有关化学的基本概念、规律和原理正确的是( )
| A. | 烧碱、冰醋酸、四氯化碳均为电解质 | |
| B. | 不同元素的原子构成的分子中只含极性共价键 | |
| C. | IA族与ⅦA族元素间可形成共价化合物或离子化合物 | |
| D. | 2NO(g)+2CO(g)=N2(g)+2CO2(g)在常温下可自发进行,则该反应的△H>0 |
14.下列实验操作和现象与结论对应关系正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 测量等浓度的Na2CO3与C6H5ONa溶液的pH | Na2CO3溶液的pH大于C6H5ONa的pH | H2CO3的酸性大于C6H5OH |
| B | 将SO2通入溴水中 | 溴水褪色 | SO2具有漂白性 |
| C | 取少量的变质FeCl2晶体于试管中,逐滴加入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色 | FeCl2未完全变质 |
| D | 向苯酚的苯溶液中加入足量NaOH溶液,振荡静置 | 分层 | 上层为苯,下层为NaOH与苯酚钠的混合溶液 |
| A. | A | B. | B | C. | C | D. | D |
4.有关化学用语的表示正确的是( )
| A. | 甲烷分子的比例模型是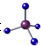 | B. | 二氧化碳的电子式: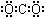 | ||
| C. | HClO的结构式为H-O-Cl | D. | 中子数为17的氯原子:${\;}_{17}^{37}$Cl |
8.下列说法中正确的是( )
| A. | 强电解质溶液总比弱电解质的导电性强 | |
| B. | 稀硫酸溶液中不存在H2SO4分子 | |
| C. | 氯化氢是电解质,所以液态氯化氢能导电 | |
| D. | 电解质溶液中只存在离子,没有分子 |
13.下列有关实验的操作、原理和现象的叙述正确的是( )
| A. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| B. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| C. | 向淀粉溶液中加入稀硫酸,加热几分钟后冷却,再加入新制的Cu(OH)2悬浊液,加热,没有砖红色沉淀生成,证明淀粉没有水解成葡萄糖 | |
| D. | 用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值 |
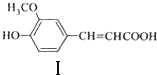 的说法,正确的是AB.
的说法,正确的是AB.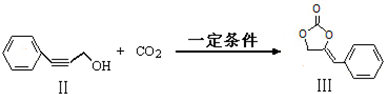
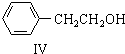 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$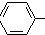 CH2CH2
CH2CH2 -CH2CH3+H2O
-CH2CH3+H2O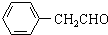 ;
;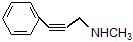 也可以和CO2发生类似反应①的反应,生成由VI,VI的结构简式为
也可以和CO2发生类似反应①的反应,生成由VI,VI的结构简式为 .
. .
.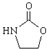 ,涉及的反应方程式为HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$
,涉及的反应方程式为HOCH2CH2NH2+CO2$\stackrel{催化剂}{→}$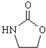 +H2O.
+H2O.