题目内容
将24.4gNaOH固体溶于水,配成100mL溶液,其密度为1.22g/mL,请回答下列问题
(1)该溶液中NaOH的物质的量浓度为__________,该溶液中NaOH的质量分数为____________;
(2)从该溶液中取出10mL,其中NaOH的物质的量浓度为__________,NaOH的质量分数为___________,溶液的密度为____________,含NaOH的质量为___________,含NaOH的物质的量为_________;
(3)将取出的10mL溶液加水稀释到100ml,稀释后溶液中NaOH的物质的量浓度为____________。
(1)6.1mol/L(2分), 20%(2分)
(2)6.1mol/L(1分), 20%(1分), 1.22g/mL(1分),2.44g(2分),0.061mol(2分)
(3)0.61mol/L(2分)
解析试题分析:(1)根据物质的量浓度、质量分数的定义进行计算:c(NaOH)=24.4g÷40g/mol÷0.1L=6.1mol?L?1;质量分数为:24.4g÷(100ml×1.22g/mL)×100%=20%。
(2)从该溶液中取出10mL,NaOH溶液的物质的量浓度、质量分数、密度不变;含氢氧化钠:n(NaOH)=0.01L×6.1mol?L?1=0.061mol;m(NaOH)=0.061mol×40g/mol=2.44g。
(3)加水溶质的物质的量不变,0.01L×6.1mol?L?1=0.1L×c(NaOH),c(NaOH)=0.61mol/L
考点:本题考查有关物质的量浓度和质量分数的计算。

过氧化钠与CO2作用,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2↑。当0.2molNa2O2与足量CO2完全反应后,下表对生成物Na2CO3和O2的描述中正确的是
| | Na2CO3的质量 | 关于O2的描述 |
| A | 21.2g | O2的摩尔质量是36g·mol-1 |
| B | 21.6g | 生成标准状况下O2的体积为2.24L |
| C | 21.6g | O2的摩尔质量是34g·mol-1 |
| D | 22.4 g | 生成标准状况下O2的体积为2.24mL |
设NA为阿伏加德罗常数,则下列说法正确的是
| A.电解精炼铜时,若阴极得到电子数为2 NA,阳极质量减少64g |
| B.200mL某硫酸盐溶液中含有1.5 NA个SO42-离子,同时含有NA个金属阳离子,该盐物质的量浓度是2.5 mol/L |
| C.常温常压下,78g Na2O2固体中所含阴、阳离子总数为4 NA |
| D.一定条件下,足量的Fe粉与浓硫酸反应,转移电子数一定为2 NA |
1molSO2和1molSO3具有相同的:①分子数;②原子数;③S原子数;④O原子数
| A.①② | B.①③ | C.①④ | D.②④ |
用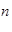 A表示阿伏加德罗常数的值。下列说法正确的是
A表示阿伏加德罗常数的值。下列说法正确的是
A.1 mol Cl-离子中含有的电子数为8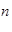 A A |
B.标准状况下,2.24 L H20中含有的分子数为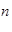 A A |
C.27g铝与足量的氧气反应,转移的电子数为3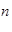 A A |
D.0.2 mo1·L-1 Ca(NO3)2溶液中含有的N03-离子数为0.4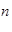 A A |
amolFe与一定量的硝酸在一定条件下充分反应,将生成的气体与标准状况下b g O2混合,恰好能被水完全吸收,则a和b的关系可能是
| A.0.5a≤b≤0.75a | B.16a≤b≤24a | C.0.2a≤b≤0.3a | D.无法确定 |
NO、NO2、O2按照一定比例通入水中,能被完全吸收,无剩余气体,若NO、NO2、O2的气体体积分别为a、b、 c、则a:b:c可能为( )
| A.1:5:2 | B.2:5:1 | C.5:1:2 | D.5:2:1 |
向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀总物质的量和加入溶液B的体积关系如图所示: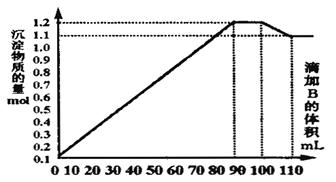
(1)当加入B溶液110 mL时,溶液中的沉淀是 (填化学式)
(2)将A.B溶液中各溶质的物质的量浓度填入下表:
| 溶 质 | Na2SO4 | BaCl2 | AlCl3 | FeCl3 |
| /mol·L-1 | | | | |
(3)写出滴加B溶液90-100mL时的离子方程式:
。