题目内容
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.1 molCH4分子中共价键总数为NA |
| B.水的摩尔质量就是NA个水分子的质量之和 |
| C.含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1mol/L |
| D.1 mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子 |
D
解析试题分析:A、甲烷含有4个C-H共价键,则1 molCH4分子中共价键总数为4NA,A不正确;B、如果质量的单位用g表示,则水的摩尔质量在数值上就是NA个水分子的质量之和,B不正确;C、过氧化钠溶解在1L水中,反应后溶液的体积不是1L,不能确定物质的量浓度,C不正确;D、镁是活泼的金属,在反应中总是失去2个电子,因此1 mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子,选项D正确,答案选D。
考点:考查阿伏加德罗常数的有关判断、应用和计算

练习册系列答案
相关题目
将铁粉和铜粉的均匀混合物,平均分成四等分,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO的体积和剩余金属的质量如下表(设硝酸的还原产物只有NO):
| 编 号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 mL | 200 mL | 300 mL | 400 mL |
| 剩余金属/g | 18.0 g | 9.6 g | 0 | 0 |
| NO体积/L | 2.24 L | 4.48 L | 6.72 L | V |
经化学定量分析,下列推断正确的是( )
A.①中溶解了5.6g Fe B.硝酸的浓度为4mol/L
C.②中溶解了9.6g Cu D.④中V=6.72 L
设nA 为阿伏加德罗常数的数值 ,下列说法正确的是(相对原子质量:O-16)
| A.常温下,8gO2和O3的混合气体中含有4nA个电子 |
| B.1molFe2+与足量的H2O2溶液反应,转移2nA个电子 |
| C.1 L 0.1 mol ·L-1NaHCO3液含有0.1nA个HCO3- |
| D.常温常压下,22.4L的NO2 和CO2混合气体含有2 nA个氧原子 |
用nA表示阿伏加德罗常数的值。下列叙述正确的是
| A.1mol?L-1的Na2CO3溶液中所含钠离子总数为2nA |
| B.标准状况下,22.4L CH4分子中含质子总数为10nA |
| C.室温下,28g乙烯和丙烯的混合物中含有的碳原子数为nA |
| D.常温常压下,33.6L氯气与足量的铝充分反应,转移电子数为3 nA |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.常温常压下,1mol甲基所含的电子总数为10nA |
| B.14g乙烯和丙烯的混合气体中含有的碳原子数为nA |
| C.标准状况下,2.24 L苯中含有0.3 nA个碳碳双键 |
| D.常温常压下,1L 0.1mol·L-1 KMnO4与足量的FeSO4反应转移电子数为3nA |
设NA为阿伏伽德罗常数的值,下列说法中正确的是
| A.常温常压下,11.2L的NO2和CO2混合气体含有NA个O原子 |
| B.标准状况下,22.4L的乙烯中含有的共用电子对数为12NA |
| C.1L0.1mo1·L-1的氨水中含有0.1NA个OH- |
| D.以石墨为电极电解氯化铜溶液时,若阳极上失去电子NA个,则阴极质量增加32g |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A.1mol Cl2通入水中,充分反应后转移电子数为NA |
| B.常温下,1.12L NO2气体含分子数为0.05NA |
| C.1L 0.5mol·L-1碳酸氢钠溶液中含离子数为NA |
| D.通常状况下16gO2和O3混合气体中含氧原子数为NA |
下列表述正确的是
| A.一氯甲烷的结构式CH3Cl |
| B.乙醇的分子式CH3CH2OH |
C.乙烷的球棍模型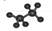 |
D.Cl-结构示意图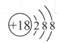 |