题目内容
把aL含(NH4)2SO4和NH4NO3的混和溶液分成两等份,一份加入b mol的烧碱并加热,恰好将全部NH4+转变成NH3放出;另一份需含c mol 的BaCl2溶液恰能完全沉淀SO42-,则原溶液中NO3-的物质的的浓度是( )
| A. (2b-4c)/a mol/L | B. (b-2c)/a mol/L |
| C. (2b-c)/a mol/L | D. (b-4c)/a mol/L |
A
混合液两等份,一份加入烧碱反应的离子方程式为
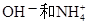 按1:1的比例反应,
按1:1的比例反应, ,另一份中加入c mol 的BaCl2反应的方程式为
,另一份中加入c mol 的BaCl2反应的方程式为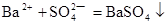 因为恰好完全沉淀所以
因为恰好完全沉淀所以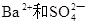 的物质的量相等,一份溶液中
的物质的量相等,一份溶液中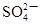 的物质的量为c mol,进而可以知道一份溶液中(NH4)2SO4的物质的量为c mol,则一份溶液中(NH4)2SO4电离出的的NH4+的物质的量为2c mol,一份溶液中的NH4+的总的物质的量为b mol,溶液中NH4+来源于(NH4)2SO4和NH4NO3,所以一份溶液中NH4NO3电离出的NH4+的物质的量为(b—2c )mol,所以一份溶液中NH4NO3电离出的NO3-的物质的量为(b—2c)mol,原溶液中NO3-的物质的量为(2b—4c )mol,所以原溶液中NO3-的物质的量浓度为(2b-4c)/a mol/L ,答案选A。
的物质的量为c mol,进而可以知道一份溶液中(NH4)2SO4的物质的量为c mol,则一份溶液中(NH4)2SO4电离出的的NH4+的物质的量为2c mol,一份溶液中的NH4+的总的物质的量为b mol,溶液中NH4+来源于(NH4)2SO4和NH4NO3,所以一份溶液中NH4NO3电离出的NH4+的物质的量为(b—2c )mol,所以一份溶液中NH4NO3电离出的NO3-的物质的量为(b—2c)mol,原溶液中NO3-的物质的量为(2b—4c )mol,所以原溶液中NO3-的物质的量浓度为(2b-4c)/a mol/L ,答案选A。
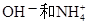 按1:1的比例反应,
按1:1的比例反应, ,另一份中加入c mol 的BaCl2反应的方程式为
,另一份中加入c mol 的BaCl2反应的方程式为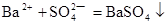 因为恰好完全沉淀所以
因为恰好完全沉淀所以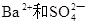 的物质的量相等,一份溶液中
的物质的量相等,一份溶液中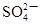 的物质的量为c mol,进而可以知道一份溶液中(NH4)2SO4的物质的量为c mol,则一份溶液中(NH4)2SO4电离出的的NH4+的物质的量为2c mol,一份溶液中的NH4+的总的物质的量为b mol,溶液中NH4+来源于(NH4)2SO4和NH4NO3,所以一份溶液中NH4NO3电离出的NH4+的物质的量为(b—2c )mol,所以一份溶液中NH4NO3电离出的NO3-的物质的量为(b—2c)mol,原溶液中NO3-的物质的量为(2b—4c )mol,所以原溶液中NO3-的物质的量浓度为(2b-4c)/a mol/L ,答案选A。
的物质的量为c mol,进而可以知道一份溶液中(NH4)2SO4的物质的量为c mol,则一份溶液中(NH4)2SO4电离出的的NH4+的物质的量为2c mol,一份溶液中的NH4+的总的物质的量为b mol,溶液中NH4+来源于(NH4)2SO4和NH4NO3,所以一份溶液中NH4NO3电离出的NH4+的物质的量为(b—2c )mol,所以一份溶液中NH4NO3电离出的NO3-的物质的量为(b—2c)mol,原溶液中NO3-的物质的量为(2b—4c )mol,所以原溶液中NO3-的物质的量浓度为(2b-4c)/a mol/L ,答案选A。
练习册系列答案
相关题目