题目内容
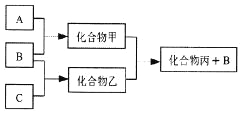
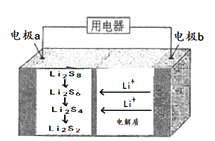
【题目】全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其电极a常用掺有石墨烯的S8材料,电极反应为:16Li+xS8=8Li2Sx(2≤x≤8)。下列说法正确的是
A. 电池工作时,外电路中流过0.02mol电子,负极材料减重0.14g
B. 电解池中加入少量硫酸增强导电性
C. 电池充电时间越长,电池中的Li2S2量越多
D. 电池工作时,负极可发生反应: 2Li2S6+2Li++2e-=3Li2S4
【答案】A
【解析】
根据电池反应16Li+xS8=8Li2Sx(2≤x≤8)可知负极锂失电子发生氧化反应,电极反应为:Li-e-=Li+,Li+移向正极,所以a是正极,发生还原反应:S8+2e-=S82-,S82-+2Li+=Li2S8,3Li2S8+2Li++2e-=4Li2S6,2Li2S6+2Li++2e-=3Li2S4,Li2S4+2Li++2e-=2Li2S2,根据电极反应式结合电子转移进行计算。
A.负极反应为:Li-e-=Li+,当外电路流过0.02mol电子时,消耗的锂为0.02mol,负极减重的质量为0.02mol×7g/mol=0.14g,A正确;
B.硫作为不导电的物质,导电性非常差,而石墨烯的特性是室温下导电最好的材料,则石墨烯的作用主要是提高电极a的导电性,但是不能加入硫酸,因为金属锂可以和硫酸之间反应,B错误;
C.充电时a为阳极,与放电时的电极反应相反,则充电时间越长,电池中的Li2S2量就会越少,C错误;
D.据分析可知正极可发生反应:2Li2S6+2Li++2e-=3Li2S4,负极上发生氧化反应,电极反应为:Li-e-=Li+,D错误;
故合理选项是A。

 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案【题目】下列图示装置和对应实验原理的描述均正确的是
A | B | C | D |
|
|
|
|
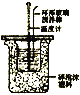
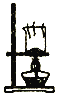
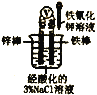
根据温度计读数的变化测定浓硫酸和NaOH溶液反应的反应热 | 加热固体NaHCO3制备少量的Na2CO3 | 验证牺牲阳极的阴极保护法,可证明铁被保护 | 根据小试管中液面的变化可判断铁钉发生了析氢腐蚀 |
A. AB. BC. CD. D
【题目】下列实验能达到相应实验目的的是
选 项 | 试剂 | 实验目的 | 实验装置 | ||
X | Y | Z | |||
A | Na2SO3 | 稀HNO3 | 品红溶液 | 证明SO2具有漂白性 |
|
B | MnO2 | 浓盐酸 | KI-淀粉溶液 | 比较Cl2与I2的氧化性强弱 | |
C | Na2CO3 | 醋酸 | Na2SiO3溶液 | 证明酸性: CH3COOH > H2CO3 >H2SiO3 | |
D | 蔗糖 | 浓硫酸 | 溴水 | 证明浓硫酸具有脱水性、氧化性 | |
A. AB. BC. CD. D