题目内容
【题目】下列反应的离子方程式书写不正确的是
A. 氯化铁与铁粉:Fe 3+ +Fe === 2Fe2+
B. 金属钠与水:2Na + 2H2O === 2Na+ + 2OH- + H2↑
C. 稀盐酸与碳酸钙:CaCO3 + 2H+ === Ca2+ + CO2 ↑ + H2O
D. 铜与浓硝酸:Cu + 4H++ 2NO3- ![]() Cu2++2NO2↑ +2H2O
Cu2++2NO2↑ +2H2O
【答案】A
【解析】A.氯化铁与铁反应生成氯化亚铁;
B.钠与水反应生成氢氧化钠和氢气;
C.稀盐酸与碳酸钙反应生成氯化钙、水和二氧化碳;
D.铜与浓硝酸反应生成硝酸铜、NO2和水。
A. 没有配平,氯化铁与铁粉反应的离子方程式为:2Fe3++Fe=3Fe2+,A错误;
B. 金属钠与水反应生成氢氧化钠和氢气:2Na+2H2O=2Na++2OH-+H2↑,B正确;
C. 稀盐酸与碳酸钙反应生成氯化钙、水和二氧化碳:CaCO3+2H+=Ca2++CO2↑+H2O,C正确;
D. 铜与浓硝酸反应生成硝酸铜、NO2和水:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O,D正确。答案选A。

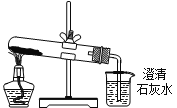
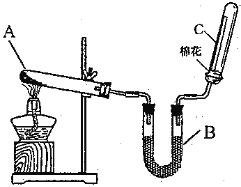
【题目】研究小组用如图装置制取Cl2 , 证明产生的气体中含有HCl. 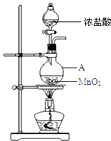
(1)仪器A的名称为;A中反应的离子方程式为;
(2)甲同学将A中产生的气体通入如表溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 | |
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为;
②不能证明产生的气体中含有HCl的实验是(填字母序号);
(3)已知将HCl气体通入饱和食盐水中有白色固体析出.乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因;
(4)已知:2S2O32﹣+I2═S4O62﹣+2I﹣ . 丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl.
I.测定X中溶解的Cl2 . 取25.00mL溶液X,加入过量KI溶液,然后用0.04molL﹣1 Na2S2O3溶液滴定生成
的I2 , 达滴定终点时消耗Na2S2O3溶液V mL.
Ⅱ.测定X中Cl元素总量.另取25.00mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl﹣ , 再用0.10molL﹣1 AgNO3溶液滴定所得溶液中的Cl﹣ .
①X中的HClO不会影响I的测定结果,原因是;
②由I、Ⅱ中实验数据可证明A中产生的气体中含有HCl,则Ⅱ中消耗0.10molL﹣1 AgNO3溶液的体积应大于mL(用含V的代数式表示).