��Ŀ����
����Ŀ��Ԫ��Xλ�ڵ������ڣ����̬ԭ�ӵ��ڲ���ȫ���������ӣ�������������Ϊ1��Ԫ��Y��̬ԭ�ӵ�3p�������5�����ӣ�Ԫ��Z��ԭ�����������������ڲ��3����Ԫ��W��̬ԭ�ӵĺ�����ӹ���16���˶�״̬��
��1������Ԫ�����ڱ��У�Ԫ��Xλ�� ����Ԫ��Yλ�ڵ� ���ڵ� �塣
��Z���������У���һ����������Ԫ���� ����Ԫ�����ƣ���
��X+�ĺ�������Ų�ʽΪ ��
��Y��W��Ԫ������������Ӧ��ˮ�������Խ�ǿ���� ���ѧʽ����
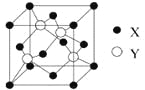
��2��X��Y���γɻ����ᄃ��ľ�����ͼ��ʾ����1�������У�X���ӵ���ĿΪ ���û�����Ļ�ѧʽΪ ��
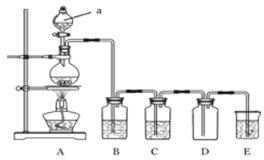
��3�������Ҵ��е��ܽ�ȣ�Z���⻯��(H2Z)����H2W������Ҫԭ���� ��
���ȶ��ԣ� H2Z H2W����������������������=����������Ҫԭ���� ��
���𰸡���1����6�֣���ds �� ��A ���� ��1s22s22p63s23p63d10��HClO4
��2��4 CuCl ��3����4�֣���ˮ�������Ҵ����Ӽ����γ������1�֣��������Ӽ��������ֲ��÷֣�����ˮ���Ӻ��Ҵ������о����ǻ�����ṹ���ƣ�1�֣�[���������һ����ɵ÷�]
���� H2O������H-O�ļ��ܴ���H2S������H-S�ļ���(����Ԫ�طǽ����Դ�����Ԫ�صķǽ����ԣ���H-O���ļ���С��H-S���ļ�����1��)
�����������������Ԫ��X λ�ڵ������ڣ����̬ԭ�ӵ��ڲ���ȫ���������ӣ����ڲ������=2+8+18=28��������������Ϊ1�����Ը�ԭ����29�����ӣ�ΪCuԪ�أ�Ԫ��Y��̬ԭ�ӵ�3p�������5�����ӣ���Y��ClԪ�أ�Ԫ��Z��ԭ�����������������ڲ��3����Ԫ������������С�ڻ����8������Z��OԪ�أ�Ԫ��W��̬ԭ�ӵĺ�����ӹ���16���˶�״̬����W��SԪ�أ�����XΪͭ��YΪ�ȣ�ZΪ����WΪ��
��1����Ԫ��YΪCl��Cl��3�����Ӳ㣬�����7�����ӣ��ʴ������ڱ��е������ڵ���A�壬Ԫ��XΪCu���������ڱ���ds����
����Ԫ����������Ϊ�ڶ����ڣ����е�һ����������Ԫ�����ʡ�
��XΪCu��Cu��ԭ������Ϊ29��Ϊ�������ڵ���B��Ԫ�أ�Cu+�ĺ�������Ų�ʽΪ1s22s22p63s23p63d10��
��Cl��S��Ԫ�����γɵ�����������Ӧ��ˮ����ֱ�ΪH2SO4��HClO4��Ԫ�صķǽ�����Խǿ�������������ˮ���������Խǿ�����ڷǽ�����Cl��S�������Խ�ǿ����HClO4��
��2����Cu��Cl���γɻ����ᄃ��ľ�����ͼ��ʾ��1��������CuΪ��8��![]() +6��
+6��![]() =4��
=4��
��Cl����Ϊ4���ʴ˾�����Cu��Cl�ĸ�����Ϊ1��1���ʻ�ѧʽΪ��CuCl��
��3����ˮ�������Ҵ����Ӽ����γ��������ˮ���Ӻ��Ҵ������о����ǻ����������Ҵ��е��ܽ�ȣ�Z���⻯��(H2O)����H2S��
��H2O������H-O�ļ��ܴ���H2S������H-S�ļ��ܣ�����ˮ���ӵ��ȶ���ǿ��H2S��