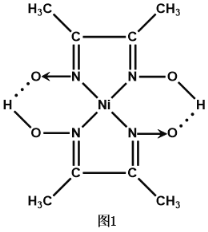
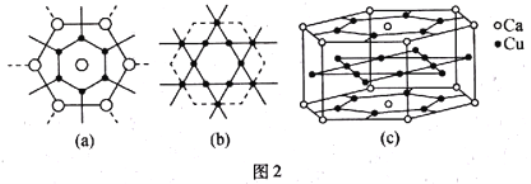
题目内容
【题目】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,某研究小组以氢氧化钠固体、浓氨水、干冰等为原料制备氨基甲酸铵的实验装置如图所示,其主要反应的原理为2NH3(g)+CO2(g)NH2COONH4(s) ΔH<0。
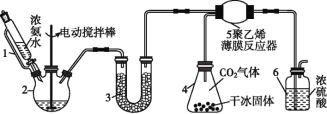
(1)仪器3中盛装的固体是____,其作用是________________。
(2)仪器6的一个作用是控制原料气按化学计量数充分反应,若反应初期观察到装置内浓硫酸中产生气泡,则应该___(填“加快”“减慢”或“不改变” )产生氨的速率。
(3)另一种制备氨基甲酸铵的反应装置(液态石蜡和CCl4均充当惰性介质)如图所示。
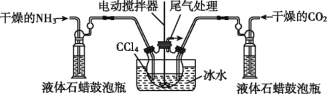
①液态石蜡鼓泡瓶的作用是________________________。
②当CCl4液体中产生较多晶体悬浮物时,立即停止反应,过滤分离得到粗产品,为了将所得粗产品干燥,可采取的方法是___(填字母)。
A.蒸馏 B.真空微热烘干 C.高压加热烘干
(4)制得的氨基甲酸铵中可能含有碳酸氢铵、碳酸铵中的一种或两种杂质(不考虑氨基甲酸铵与水的反应)。
①设计方案进行成分探究,请填写表中空格。
限选试剂:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
实验步骤 | 预期现象和结论 |
步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解 | 得到无色溶液 |
步骤2:向试管中加入过量的BaCl2溶液,静置 | 若溶液不变浑浊,则证明固体中不含碳酸铵 |
步骤3:向试管中继续加入____________ | _____________,则证明固体中含有碳酸氢铵 |
②根据①的结论,取15.8 g氨基甲酸铵样品,用足量氢氧化钡溶液充分处理后,过滤洗涤、干燥,测得沉淀的质量为1.97 g。则样品中氨基甲酸铵的质量分数为____。
【答案】碱石灰 干燥氨,防止仪器5中生成的氨基甲酸铵水解 加快 通过观察气泡,调节NH3与CO2的通入比例(或通过观察气泡,控制通入NH3与CO2的速率) B 少量澄清石灰水 若溶液变浑浊 0.95(或95%)
【解析】
(1)氨气由浓氨水与碱制备,由于氨基甲酸铵易水解,U型管内用碱石灰干燥氨气,防止仪器5中生成的氨基甲酸铵水解,在5中反应得到氨基甲酸铵,6中稀硫酸进行尾气处理,防止剩余的氨气污染空气;
(2)若反应初期观察到装置内稀硫酸溶液中产生气泡,说明有二氧化碳排出,通入氨气的量不足,应该适当加快产生氨气的流速;
(3)①通过观察气泡,控制通入NH3与CO2的速率,使二者反应更充分;
②氨基甲酸铵受热易分解,采取减压低温烘干,即真空微热烘干,答案选B;
(4)①步骤3检验碳酸氢铵,需要检验碳酸氢根离子,继续加入少量澄清石灰水,若溶液变浑浊,则证明固体中含有碳酸氢铵;
②根据①的结论,取15.8 g氨基甲酸铵样品,用足量氢氧化钡溶液充分处理后,过滤洗涤、干燥,测得沉淀的质量为1.97 g,沉淀为碳酸钡,碳酸钡的物质的量=![]() =0.01mol,由碳原子守恒,可知碳酸氢铵的物质的量为0.01mol,故碳酸氢铵的质量为=0.01mol×79g/mol=0.79g,故氨基甲酸铵的质量分数=
=0.01mol,由碳原子守恒,可知碳酸氢铵的物质的量为0.01mol,故碳酸氢铵的质量为=0.01mol×79g/mol=0.79g,故氨基甲酸铵的质量分数=![]() ×100%=95%(或0.95)。
×100%=95%(或0.95)。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案