题目内容
( 7分) A—J是中学化学常见的物质,它们之间的转化关系如下图所示(部分产物已略去)。已知A是一种高熔点物质,D是一种红棕色固体。
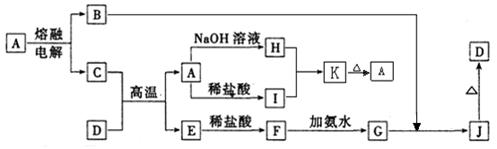
请回答下列问题:
(1)固体A的晶体类型为___________,K的化学式为 。
(2)C与D在高温下的反应在冶金工业上称为 反应。
(3)G→J的化学方程式为 。
(4)A→H的离子方程式为 。
(5)I的水溶液pH_____7(填“>”、“<”或“=”),原因是 (用离子方程式表示)。

请回答下列问题:
(1)固体A的晶体类型为___________,K的化学式为 。
(2)C与D在高温下的反应在冶金工业上称为 反应。
(3)G→J的化学方程式为 。
(4)A→H的离子方程式为 。
(5)I的水溶液pH_____7(填“>”、“<”或“=”),原因是 (用离子方程式表示)。
(1)离子晶体(1分) Al(OH)3(1分)
(2)铝热反应(1分)(3)4Fe(OH)2+O2+2H2O=4Fe(OH)3(1分)
(4)Al2O3+2OH—=2AlO2—+H2O(1分)
(5)< (1分) Al3++3H2O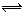 Al(OH)3+3H+(1分)
Al(OH)3+3H+(1分)
(2)铝热反应(1分)(3)4Fe(OH)2+O2+2H2O=4Fe(OH)3(1分)
(4)Al2O3+2OH—=2AlO2—+H2O(1分)
(5)< (1分) Al3++3H2O
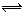 Al(OH)3+3H+(1分)
Al(OH)3+3H+(1分)试题分析:D是一种红棕色固体,为Fe2O3,C、D的反应为铝热反应,C为铝,A是一种高熔点物质,即可得A为Al2O3,B为O2,又可推得E为Fe,F为FeCl2,G为Fe(OH)2,和氧气反应,得J为Fe(OH)3,加热分解得D为Fe2O3。Al2O3和NaOH反应的H为NaAlO2 , Al2O3和稀盐酸反应得I为AlCl3,Al2O3和AlCl3发生双水解反应,得K为Al(OH)3,加热又得A为Al2O3。
点评:在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质在题中的转换关系推导剩余的物质,最后进行验证即可

练习册系列答案
相关题目
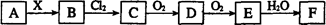


 请回答下列问题:
请回答下列问题:

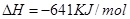


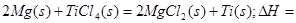 ____________
____________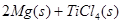

 在Ar气氛中进行的理由是________
在Ar气氛中进行的理由是________