题目内容
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )。
A.NH4Cl NH3↑+HCl↑
NH3↑+HCl↑
B.NH3+CO2+H2O=NH4HCO3
C.2NaOH+Cl2=NaCl+NaClO+H2O
D.2Na2O2+2CO2=2Na2CO3+O2
D
【解析】本题主要考查学生对化学反应实质即旧化学键的断裂与新化学键的生成的理解程度。A选项中没有非极性共价键的断裂与形成;B选项中没有离子键的断裂,也没有非极性共价键的断裂与生成;C选项中没有非极性共价键的生成,只有D选项中反应前有Na+与O22-的离子键,O—O的非极性键,C—O间的极性键的断裂,反应后有成盐的离子键,氧分子中O—O非极性键及C—O极性键的形成,符合题意。

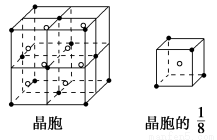
下列数据对应物质的熔点,据此作出下列判断中错误的是( )。
Na2O | NaCl | AlF3 | AlCl3 |
920 ℃ | 801 ℃ | 1 292 ℃ | 190 ℃ |
BCl3 | Al2O3 | CO2 | SiO2 |
-107 ℃ | 2 073 ℃ | -57 ℃ | 1 723 ℃ |
A.铝的化合物的晶体中有离子晶体
B.表中只有BCl3和干冰是分子晶体
C.同族元素的氧化物可形成不同类型的晶体
D.不同族元素的氧化物可形成相同类型的晶体
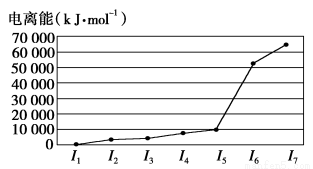
A、B、C、D、E五种元素,A元素的周期数、主族数、原子序数相同;B的基态原子核外有3种能量不同的原子轨道,且每种轨道中的电子数相同;C元素的电离能如图所示;D元素的价电子构型为nsnnpn+2;E是第4周期的过渡元素,血红蛋白中的E元素与BD形成的配位键比与D2形成的配位键强。E单质与BD形成的配合物E(BD)5,常温下呈液态,熔点为-20.5℃,沸点为103 ℃,易溶于非极性溶剂。
C元素的电离能
(1)E(BD)5晶体属于________(填晶体类型)。
(2)A元素和B元素组成的化合物分子之间________(填“能”或“不能”)形成氢键。
(3)基态E原子的电子排布式为___________________________________ 。
(4)B、C、D三种元素的电负性由大到小的顺序是________(填元素符号)。
(5)C2和B2A2的分子中根据电子云重叠的方式不同,都包含的共价键类型有________。
(6)已知原子数和电子数相同的微粒叫等电子体,等电子体的结构相似。根据
下表数据,说明BD分子比C2分子活泼的原因_____________________________。
| X—Y | X=Y | X≡Y |
BD的键能/kJ·mol-1 | 357.7 | 798.9 | 1 071.9 |
C2的键能/kJ·mol-1 | 154.8 | 418.4 | 941.7 |