题目内容
【题目】已知断开1molCl2(g)中的化学键需要吸收242.7kJ的能量。根据反应H2(g)+Cl2(g)=2HCl(g)的能量变化示意图,下列说法不正确的是( )
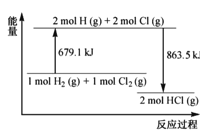
A.H2(g)+Cl2(g)=2HCl(g) ΔH=-184.4kJ·mol-1
B.HCl(g)=![]() H2(g)+
H2(g)+![]() Cl2(g) ΔH=92.2kJ·mol-1
Cl2(g) ΔH=92.2kJ·mol-1
C.断开1molH2(g)中的化学键需要吸收436.4kJ的能量
D.H2(g)和Cl2(g)形成1molHCl(g)释放863.5kJ的能量
【答案】D
【解析】
A.已知断开1molCl2(g)中的化学键需要吸收242.7kJ的能量,1molH2(g)+1molCl2(g)=2molH+2molCl,吸收679.1kJ能量,2molH+2molCl=2molHCl(g)放出863.5kJ能量,所以H2(g)+Cl2(g)=2HCl(g) ΔH=-184.4kJ·mol-1,故A不符合题意;
B.根据盖斯定律以及A分析可知,HCl(g)=![]() H2(g)+
H2(g)+![]() Cl2(g) ΔH=92.2kJ·mol-1,故B不符合题意;
Cl2(g) ΔH=92.2kJ·mol-1,故B不符合题意;
C.断开1molCl2(g)中的化学键需要吸收242.7kJ的能量,则断开1molH2(g)中的化学键需要吸收679.1kJ-242.7kJ=436.4kJ,故C不符合题意;
D.由A可知,H2(g)和Cl2(g)形成1molHCl(g)释放92.2kJ的能量,故D符合题意;
故答案为:D。

练习册系列答案
相关题目