题目内容
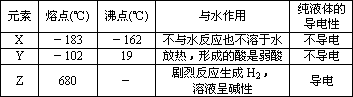
碱金属元素可形成离子型氢化物,下表是同一短周期元素X、Y、Z三种元素氢化物的某些性质
则这三种元素的原子序数从大到小的排列顺序为( )
| 元素 | 熔点(℃) | 沸点(℃) | 与水作用 | 纯液体的导电性 |
| X | -183 | -162 | 不与水反应也不溶于水 | 不导电 |
| Y | -102 | 19 | 放热,形成的酸是弱酸 | 不导电 |
| Z | 680 | - | 剧烈反应生成H2,溶液呈碱性 | 导电 |
| A、X、Y、Z |
| B、Z、X、Y |
| C、Y、X、Z |
| D、Z、Y、X |
分析:同周期从左向右金属性在减弱,金属性越弱,其金属氢化物的共价性越大,被水分解的难度也就越大.对非金属氰化氢来说,非金属性越强,键的极性越大,根据相似相溶可知,越易溶于水.
解答:解:同周期从左向右金属性在减弱,金属性越弱,其金属氢化物的共价性越大,被水分解的难度也就越大.对非金属氰化氢来说,非金属性越强,键的极性越大,根据相似相溶可知,越易溶于水,由同一短周期元素X、Y、Z三种元素氢化物的某些性质可知,Z的金属性最强,Y的非金属性最大,X介于二者之间,
则原子序数为Y>X>Z,
故选C.
则原子序数为Y>X>Z,
故选C.
点评:本题考查位置、结构、性质,明确同周期元素金属性、非金属性的变化是解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
|
碱金属元素可形成离子型氢化物,下表是同一短周期元素X、Y、Z三种元素氢化物的某些性质
则这三种元素的原子序数从大到小的排列顺序为 | |
| [ ] | |
A. |
X、Y、Z |
B. |
Z、X、Y |
C. |
Y、X、Z |
D. |
Z、Y、X |
有人认为处于第IA族的氢元素也可以放在其他主族中,下列有关说法不正确的是
| A.根据氢元素再得一个电子形成稳定结构可以放在第ⅦA族 |
| B.根据氢元素可与碱金属元素形成离子化合物NaH,可以放在ⅦA族 |
| C.氢元素应放在氟元素的上边 |
| D.根据氢元素最高正价与最低负价的绝对值相等可以放在ⅣA族 |