题目内容
【题目】我国化工专家侯德榜的“侯氏制碱法” 又叫“联合制碱法”以NaCl、NH3、CO2等为原料先制得NaHCO3,进而生产出纯碱Na2CO3,有关反应的化学方程式:
(1)______________。
(2)______________。
【答案】NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl 2NaHCO3![]() Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
【解析】
对于非氧化还原反应,先写出主要的反应物及生成物,根据客观事实和原子守恒即可书写出正确的化学方程式,碳酸氢钠受热易分解成为碳酸钠、二氧化碳和水,从而把化学方程式都写出来。
(1)以NaCl、NH3、CO2等为原料先制得NaHCO3,该反应的化学方程式:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(2)以 NaHCO3为原料生产出纯碱Na2CO3,该反应的化学方程式为:2NaHCO3![]() Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。

【题目】N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g)![]() 4NO2(g)+O2(g) ΔH >0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表,下列说法正确的是
4NO2(g)+O2(g) ΔH >0。T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表,下列说法正确的是
时间/s | 0 | 500 | 1 000 | 1 500 |
c(N2O5)/mol·L-1 | 5.00 | 3.50 | 2.50 | 2.50 |
A. 500 s内NO2的生成速率为3.00×10-3 mol·L-1·s-1
B. T1温度下该反应平衡时N2O5的转化率为50%
C. 达平衡后其他条件不变,将容器体积压缩到原来的![]() ,c(N2O5)<5.00 mol·L-1
,c(N2O5)<5.00 mol·L-1
D. T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2
【题目】Ⅰ.常温下有浓度均为0.1 mol/L的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O
(1)这四种溶液中水的电离程度由大到小的顺序是___________________(用序号填写)。
(2)等体积混合③和④的溶液中离子浓度的大小顺序是:__________________________。
(3)②溶液中存在的质子守恒关系:c(OH-)=___________________________。
(4)向④中加入少量氯化铵固体,溶液中c(H+)______(填“增大”、“减小”或“不变”)
(5)取10mL溶液③,加水稀释到100mL,则该溶液中由水电离出的c(H+)约为________。
Ⅱ.普通泡沫灭火器内的玻璃筒里盛有Al2(SO4)3溶液,铁筒中盛有NaHCO3溶液,当意外失火时,打开泡沫灭火器使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为:______________________________________,不能把Al2(SO4)3溶液盛放在铁筒中的主要原因是______________________________________________________。
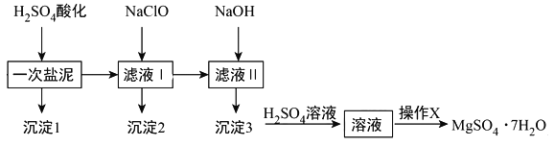
Ⅲ.某工厂的电镀污泥中含有铜、铁等金属化合物。为实现资源的回收利用并有效防止环境污染,设计如下工艺流程:

沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 2.3 | 7.6 | 4.4 |
完全沉淀的pH | 3.2 | 9.7 | 6.4 |
(1)酸浸后加入H2O2的目的是___________________,调pH的最适宜范围为__________。
(2)调pH过程中加入的试剂最好是___________(填标号)。
A. NaOH B. CuO C.NH3·H2O D.HCl