题目内容
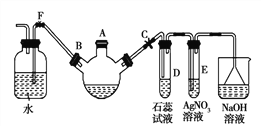
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________。
(2)从油水混合物中分离出植物油,选择装置________,该分离方法的名称为________。
(3)装置A中①的名称是________,进水的方向是从________(填“上”或“下”)口进水。装置B在分液时上层液体从________(填仪器名称)的________(填“上”或“下”)口流出。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
粗盐中含Ca2+、Mg2+、Fe3+、![]() 等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发
正确的操作顺序是________(填选项字母)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦
c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
【答案】D A B 分液 冷凝管 下 分液漏斗 上 ad
【解析】
(1). 蒸发可以实现易溶于水的固体和水的分离,从氯化钾溶液中得到氯化钾固体可用蒸发的方法,装置选D;因蒸馏可以实现水中难挥发性杂质和水的分离,则除去自来水中的Cl─等杂质,可用蒸馏的方法,装置选A,故答案为:D;A;
(2). 植物油与水互不相溶,可用分液法分离,装置选B,故答案为:B;分液;
(3). 装置A中①的名称是冷凝管,使用时下口进水上口出水,装置B在分液时,上层液体从分液漏斗的上口倒出,故答案为:冷凝管;下;分液漏斗;上;
(4). 除去粗盐中的可溶性杂质:Mg2+、Ca2+、Fe3+、SO42时,可以加入过量NaOH(除去镁离子和铁离子):Mg2++2OH-=Mg(OH)2↓,Fe3++3OH-═Fe(OH)3↓,加入过量BaCl2(除去硫酸根离子):SO42+Ba2+=BaSO4↓,加入过量Na2CO3(除去钙离子和多余的钡离子):Ca2++CO32=CaCO3↓,CO32+Ba2+=BaCO3↓,碳酸钠必须加在氯化钡之后,氢氧化钠和氯化钡可以颠倒加入的顺序,过滤后调节溶液的pH等于7,然后再蒸发即可,所以顺序为⑤③②①⑥④⑦或⑤②③①⑥④⑦;故选ad。