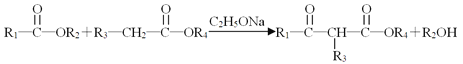��Ŀ����
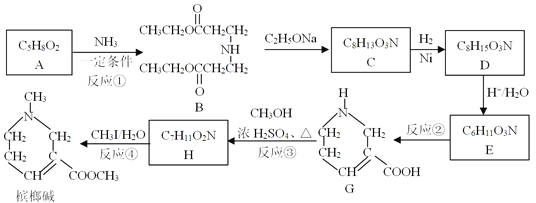
����Ŀ������д�����з�Ӧ�����ӷ���ʽ��
��1�����������ڴ������ܽ������ݲ�����______________________________________��
��2��CuSO4��Һ��Ba(OH)2��Һ��ϣ�________________________________________��
������һ��ϡ��Һ�������������֣���Һ��ɫ�����壬����ܺ���![]() ��Na+��
��Na+��![]() ��H+��
��H+��![]() ��
��![]() ��Cl�������е������֡�Ȼ�����������·�������ȷ����Щ�����Ƿ���ڡ�
��Cl�������е������֡�Ȼ�����������·�������ȷ����Щ�����Ƿ���ڡ�
����ʯ����Һ������Һʱ����Һ�Ժ�ɫ��
��ȡ2 mL��Һ��BaCl2��Һ��ϡ������м��飬��������˰�ɫ������
�����������õĻ�����־��ú�ȡ���ϲ�����Һ����AgNO3��Һ��ϡ������м��飬����������˰�ɫ������
��ش��������⣺
��1��ԭ��Һ��һ�����ڵ�������__________��һ�������ڵ�������____________��
��2��������ʵ������У��д���IJ�����_________������ţ����Ըô�������ķ����ǣ�Ҫ������ϸ��˵����_________________________________________________________��
��3����ĿǰΪֹ�����ܿ϶���ԭ��Һ���Ƿ���ڵ�������____________��
���𰸡�������1��CaCO3+2CH3COOH===Ca2++2CH3COO+H2O+CO2����3�֣�
��2��Cu2++![]() +Ba2++2OH===BaSO4��+Cu(OH)2����3�֣�
+Ba2++2OH===BaSO4��+Cu(OH)2����3�֣�
������1��H+��![]() ��1�֣�
��1�֣� ![]() ��
��![]() ��1�֣�
��1�֣�
��2������1�֣� ��ȡԭ��Һ2 mL����AgNO3��Һ��ϡ������м��飨1�֣�
��3��Na+��![]() ��Cl��1�֣�
��Cl��1�֣�
��������������ʯ����Һ��⣬��Һ�Ժ�ɫ��˵����Һ����H+����H+�Ͳ�����![]() ��
��![]() ����BaCl2��Һ��ϡ�������ʱ�����˰�ɫ������˵����Һ����
����BaCl2��Һ��ϡ�������ʱ�����˰�ɫ������˵����Һ����![]() ������BaCl2��Һ�б����ͺ���Cl�����Ե����������Ǵ���ģ�Ӧ��ȡԭ��Һ����Cl�ļ��飬��ȷ����Һ���Ƿ����Cl��
������BaCl2��Һ�б����ͺ���Cl�����Ե����������Ǵ���ģ�Ӧ��ȡԭ��Һ����Cl�ļ��飬��ȷ����Һ���Ƿ����Cl��