题目内容
【题目】某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯
己知: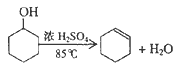
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品
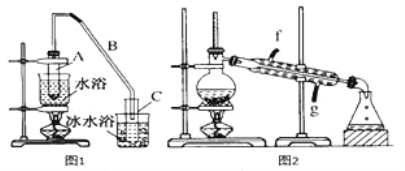
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是____________;
②试管C置于冰水浴中的目的是______________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环乙烯在______层(填上或下),分液后用___________(填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图2所示装置蒸馏,冷却水从________口进入,收集产品时,控制的温度应在______左右。
(3)以下区分环己烯精品和租品的方法,合理的是_____________。
a.用酸性高锰酸钾溶液 b.用NaOH溶液 c.测定沸点
【答案】防止暴沸 冷凝 进一步冷却,防止环乙烯挥发 上层 c g 83℃ c
【解析】
(1)①反应需要加热,A中碎瓷片的作用是防止暴沸,导管B比较长,能增加与空气的接触面积,其作用是导气和将生成的气体物质冷凝回流;
②试管C置于冰水浴中的目的是进一步冷却,降低环己烯蒸气的温度,使其液化,防止环己烯挥发;
(2)①环己烯不溶于水,且密度比水小,振荡、静置、分层后环己烯在上层;由于分液后环己烯粗品中还含有少量的酸和环己醇,联想制备乙酸乙酯提纯产物时用c(Na2CO3溶液)洗涤可除去酸,不能用酸性高锰酸钾,否则会氧化环己烯,所以分液后用c洗涤;
②再将环乙烯按图2所示装置蒸馏,为了使冷凝的效果更好,冷却水从冷凝管的下口即g口进入;根据题干表格提供的数据,环己烯的沸点为83℃,收集产品时,控制的温度应在环己烯的沸点83℃左右;
(3)根据混合物没有固定的沸点,而纯净物有固定的沸点,通过测定环己烯粗品和环己烯精品的沸点,也可判断产品的纯度;使用氢氧化钠没有明显的实验现象,无法区分,无论粗品还是精品中都含有环己烯,环己烯具有还原性,能够使高锰酸钾、溴水褪色,所以不能用来区别二者,合理的是c。