题目内容
3.A元素的最高正价是+4,A原子次外层上有2个电子,A原子的电子排布式是1s22s22p2.分析 A元素的最高正价是+4价,原子次外层上有2个电子的元素是碳.
解答 解:A元素的最高正价是+4价,原子次外层上有2个电子的元素是碳,C的基态原子的电子排布式是:1s22s22p2,故答案为:1s22s22p2.
点评 本题考查原子核外电子排布知识,侧重于基础知识的考查,为高考高频考点,注意相关基础知识的积累,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,22.4L氧气所含的原子数为2NA | |
| B. | 17g的OH-离子中含有的电子数为9NA | |
| C. | 常温常压下,44gCO2含有的氧原子数为2NA | |
| D. | 标准状况下,11.2L四氯化碳所含分子数为0.5NA |
11.pH=a的某电解质溶液中,插入两只惰性电极,通直流电一段时间后,停止电解,取出电极,将溶液摇匀,测得溶液的pH>a,则该电解质溶液是( )
| A. | K2SO4 | B. | NaOH | C. | NaCl | D. | AgNO3 |
18.下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 浓度均为0.1 mol•L-1的氨水和盐酸等体积混合后:c(H+)=c(OH-)+c(NH3•H2O) | |
| B. | 等浓度的碳酸钠、碳酸氢钠溶液混合后:c(CO${\;}_{3}^{2-}$)<c(HCO${\;}_{3}^{-}$) | |
| C. | 在NaHB溶液中一定有:c(Na+)=c(HB-)+2c(B2-) | |
| D. | Na2CO3溶液中:2c(Na+)=c(CO${\;}_{3}^{2-}$)+c(HCO${\;}_{3}^{-}$)+c(H2CO3) |
8.为了比较铁和铜金属活动性强弱,某研究小组的同学设计了如下一些方案,并将实验结果记录如下:
能根据以上各种现象或产物证明铁的金属活动性比铜强的方案一共有( )
能根据以上各种现象或产物证明铁的金属活动性比铜强的方案一共有( )
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气中燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别放入热浓硫酸中 | 产物分别为Fe2(SO4)3和CuSO4 |
| ④将铁片和铜片分别置于稀硫酸溶液中 | 铁片上有气泡,铜片上不产生气泡 |
| ⑤将铁片和铜片同时插入盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
15.如图R、W、X、Y、Z为五种物质,若箭头表示能一步转化的常见反应,则其中常温下能实现图示转化关系的是( )
| 选项 | R | W | X | Y | Z | 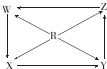 |
| A | Si | SiO2 | H2SiO2 | Na2SiO2 | SiCl4 | |
| B | Na | Na2O | Na2O2 | Na2CO3 | NaOH | |
| C | Fe | Fe(OH)2 | FeCl3 | FeCl3 | Fe(NO4)3 | |
| D | Al | NaAlO2 | Al2(SO4)3 | AlCl3 | Al(NO4)3 |
| A. | A | B. | B | C. | C | D. | D |
12.下列说法正确的是( )
| A. | 常温下浓硫酸能使铝发生钝化,可在常温下用铝制贮罐贮运浓硫酸 | |
| B. | 取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+ | |
| C. | 检验Fe(NO3)2晶体是否已氧化变质,将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 | |
| D. | 常温下将Al片放入浓硝酸中,无明显变化,所以Al与浓硝酸不反应 |
13.下列各组物质中,氮元素既有氧化性又有还原性的-组物质是( )
| A. | NH3、N2、NO、NO2 | B. | NO、NO2、N2O、N2O3 | ||
| C. | N2、N2O、NO2、N2O5 | D. | NH3、NO2、N2O4、HNO3 |