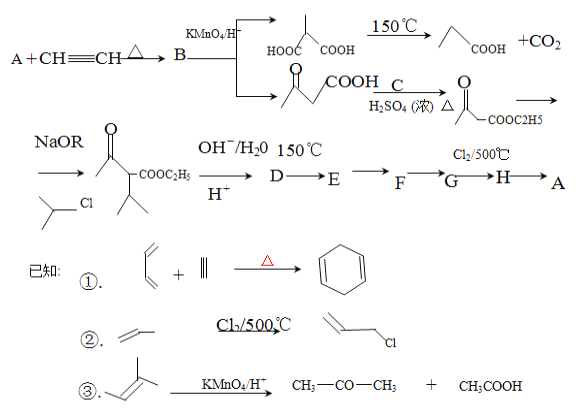
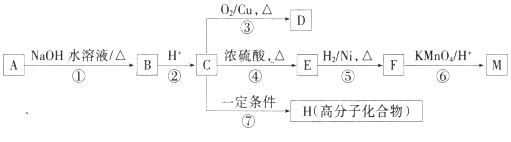
题目内容
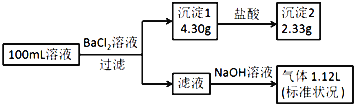
【题目】下列各组混合物构成的溶液,加入Ba(OH)2 溶液,生成沉淀的物质的量变化趋势符合图示的( )
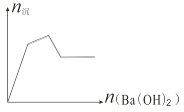
A. Al2(SO4)3、AlCl3 B. KAl(SO4)2、Al2(SO4)3 C. Al2(SO4)3、Fe2(SO4)3 D. FeCl3、AlCl3
【答案】A
【解析】
D中沉淀为氢氧化铁和氢氧化铝,沉淀的物质的量应是先增大后减小,最后不变,图像不符合,D错误;由反应Al2(SO4)3+ 3Ba(OH)2=2Al(OH)3↓+3BaSO4↓可知,若只有Al2(SO4)3,沉淀的物质的量也是先增大后减小,最后不变,图像不符合;若Al2(SO4)3中混有Fe2(SO4)3,结果与Al2(SO4)3一样,C不符合图像要求;若Al2(SO4)3中混有AlCl3,则会在沉淀的物质的量增大的过程中出现拐点,即A符合;若Al2(SO4)3中混有KAl(SO4)2 ,由于2KAl(SO4)2+ 3Ba(OH)2=2Al(OH)3↓+3BaSO4↓+K2SO4,KAl(SO4)2+ 2Ba(OH)2=KAlO2+2 BaSO4↓+2H2O,随着Ba(OH)2的加入,生成的沉淀的物质的量反而减小,和图像不符合,即B错误;
正确选项A。

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】(1)已知在常温常压下:
①CH3OH(l)+O2(g)===CO(g)+2H2O(g) ΔH=-354.8 kJ·mol-1
②2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ·mol-1
③H2O(g)===H2O(l) ΔH=-44.0 kJ·mol-1
则表示CH3OH(l)燃烧热的热化学方程式为______________________________________。
(2)由甲醇、氧气和NaOH溶液构成的新型手机电池,充电一次可使手机连续使用一个月。
①该电池负极的电极反应式为________________________________________________。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl- | SO42- |
c/(mol·L-1) | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)。阳极上最先发生的反应为___________________________;从各阶段的电解总反应方程式来看,最初是电解__________(填写化学式,下同)溶液,然后是电解________溶液,最后是电解H2O。