题目内容
已知常温下,0.1mol/L的一元酸HA溶液的pH>1;0.1mol/L的一元碱MOH溶液中 ,将此两种溶液等体积混合,混合夜中,离子浓度关系不正确的是( )
,将此两种溶液等体积混合,混合夜中,离子浓度关系不正确的是( )
A.c(OH﹣)=c(HA)+c(H+)
B.c(M+)>c(A﹣)>c(OH﹣)>c(H+)
C.c(A﹣)>c(M+)>c(H+)>c(OH﹣)
D.c(M+)+c(H+)=c(A﹣)+c(OH﹣)
C
解析试题分析:0.1mol/L的一元酸HA溶液的pH>1,则酸部分电离,为弱酸;0.1mol/L的一元碱MOH溶液中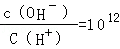 ,结合水的离子积常数知,
,结合水的离子积常数知, =1012,则溶液中氢氧根离子浓度=0.1mol/L,所以碱为强碱,二者等体积混合时恰好反应生成强碱弱酸盐,根据盐的性质及电荷守恒分析解答.
=1012,则溶液中氢氧根离子浓度=0.1mol/L,所以碱为强碱,二者等体积混合时恰好反应生成强碱弱酸盐,根据盐的性质及电荷守恒分析解答.
解:0.1mol/L的一元酸HA溶液的pH>1,则酸部分电离,为弱酸;0.1mol/L的一元碱MOH溶液中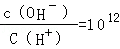 ,结合水的离子积常数知,
,结合水的离子积常数知, =1012,则溶液中氢氧根离子浓度=0.1mol/L,所以碱为强碱,二者等体积混合时恰好反应生成强碱弱酸盐,
=1012,则溶液中氢氧根离子浓度=0.1mol/L,所以碱为强碱,二者等体积混合时恰好反应生成强碱弱酸盐,
A.根据质子守恒得c(OH﹣)=c(HA)+c(H+),故A正确;
B.该溶液的溶质是盐,且该盐是强碱弱酸盐其溶液呈碱性,则c(OH﹣)>c(H+),根据电荷守恒得c(M+)>c(A﹣),盐溶液中酸根离子浓度大于氢氧根离子浓度,所以该溶液中离子浓度大小顺序是c(M+)>c(A﹣)>c(OH﹣)>c(H+),故B正确;
C.该溶液的溶质是盐,且该盐是强碱弱酸盐其溶液呈碱性,则c(OH﹣)>c(H+),根据电荷守恒得c(M+)>c(A﹣),盐溶液中酸根离子浓度大于氢氧根离子浓度,所以该溶液中离子浓度大小顺序是c(M+)>c(A﹣)>c(OH﹣)>c(H+),故C错误;
D.根据电荷守恒得c(M+)+c(H+)=c(A﹣)+c(OH﹣),故D正确;
故选:C.
考点:离子浓度大小的比较
点评:本题考查了混合溶液定性判断,正确判断酸及碱的强弱是解本题关键,结合溶液中的溶质及电荷守恒来分析解答即可,难度中等.

 名校课堂系列答案
名校课堂系列答案