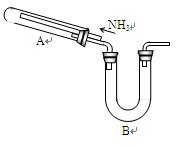
题目内容
将32 g Cu与140 mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答:?
(1)NO的物质的量为 mo
mo L,NO2的物质的量为 moL。
L,NO2的物质的量为 moL。
(2)产生的气体全部释放后,向溶液中加入V mL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的浓度为 mol/L。
(3)欲使铜与硝酸 反应生成的气体在氢氧化钠溶液中全部转化为NaNO3,至少需要质量分数为30%的双氧水 g。
反应生成的气体在氢氧化钠溶液中全部转化为NaNO3,至少需要质量分数为30%的双氧水 g。
(1)NO的物质的量为
 mo
mo L,NO2的物质的量为 moL。
L,NO2的物质的量为 moL。(2)产生的气体全部释放后,向溶液中加入V mL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部转化为沉淀,则原硝酸溶液的浓度为 mol/L。
(3)欲使铜与硝酸
 反应生成的气体在氢氧化钠溶液中全部转化为NaNO3,至少需要质量分数为30%的双氧水 g。
反应生成的气体在氢氧化钠溶液中全部转化为NaNO3,至少需要质量分数为30%的双氧水 g。(1)0.25 0.25 (2)(0.5+aV×10-3)/0.14 (3)56.7
略

练习册系列答案
相关题目
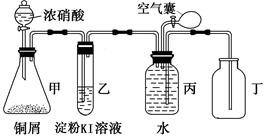
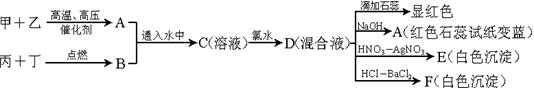
 3Cu + N2 +3H2O
3Cu + N2 +3H2O