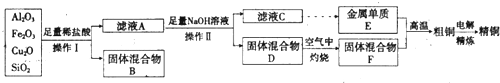
题目内容
12.下列反应的离子方程式正确的是( )| A. | 硫化亚铁中加入盐酸:S2-+2H+═H2S↑ | |
| B. | 向Ca(ClO)2溶液中通入SO2:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| C. | 硫酸铝溶液和少量苏打溶液反应:3H2O+Al3++3CO32-═3HCO3-+Al(OH)3↓ | |
| D. | 钠和冷水反应:2Na+2H2O═2Na++H2↑+2OH- |
分析 A.硫化亚铁为沉淀,保留化学式;
B.次氯酸具有氧化性,能够氧化亚硫酸根离子;
C.发生双水解生成二氧化碳、氢氧化铝;
D.钠和冷水反应生成氢氧化钠和氢气.
解答 解:A.硫化亚铁中加入盐酸,离子方程式:FeS+2H+═H2S↑+Fe2+,故A错误;
B.向次氯酸钙溶液通入SO2,离子方程式:Ca2++2ClO?+SO2+H2O=CaSO3↓+2HClO,生成的次氯酸具有氧化性,能够氧化亚硫酸根离子,故B错误;
C.硫酸铝溶液和少量苏打溶液反应,离子方程式:3H2O+2Al3++3CO32-═2Al(OH)3↓+3CO2↑,故C错误;
D.钠和冷水反应,离子方程式:2Na+2H2O═2Na++H2↑+2OH-,故D正确;
故选:D.
点评 本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 1L1mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 88g乙酸乙酯中存在的共价键总数为14NA | |
| C. | 加热时,含2molH2SO4的浓硫酸与足量铜反应,转移的电子数为2NA | |
| D. | 1mol羟基所含的电子数为10NA |
1.将5.1g镁铝合金溶于70mL 4mol/L硫酸中,当合金完全溶解后,再加入70mL 8mol/L的NaOH溶液,得沉淀的质量为13.6g,则加入硫酸时,产生H2的物质的量为( )
| A. | 0.2 mol | B. | 0.25 mol | C. | 0.3 mol | D. | 0.35 mol |
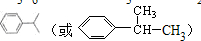
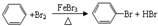 ,预测该芳香烃能(填“能”或“不能”)发生该类反应.
,预测该芳香烃能(填“能”或“不能”)发生该类反应.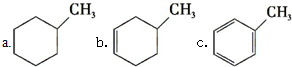
 c.
c.

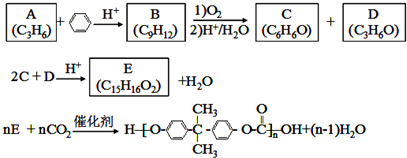
 ;D有多种同分异构体,其中含有醛基的是CH3CH2CHO.按官能团分类E为酚.
;D有多种同分异构体,其中含有醛基的是CH3CH2CHO.按官能团分类E为酚. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$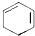 +2NaBr+2H2O.
+2NaBr+2H2O.