题目内容
10.关于化学反应的说法中错误的是( )| A. | 如图所示的反应为放热反应 | |
| B. | 化学反应中有物质变化也有能量变化 | |
| C. | 化学反应具有方向性 | |
| D. | 化学键断裂吸收能量,化学键生成放出能量 |
分析 A、当反应物的总能量小于生成物的总能量时,反应吸热;
B、化学变化一定有新物质生成,且一定伴随能量的变化;
C、△H<0,△s>0的反应更易自发进行;
D、原子比分子更不稳定.
解答 解:A、当反应物的总能量小于生成物的总能量时,反应吸热,故此反应为吸热反应,故A错误;
B、化学变化一定有新物质生成,且一定伴随能量的变化,不存在既不吸热也不放热的反应,故B正确;
C、△H<0,△s>0的反应更易自发进行,△H>0,△s<0的反应不能自发进行,即反应有方向性,故C正确;
D、原子比分子更不稳定,能量更高,故化学键断开变为原子,能量升高,要吸收能量;形成化学键能量降低,会放出能量,故D正确.
故选A.
点评 本题考查了化学反应中的能量的变化情况、化学键的断裂形成对能量的要求,难度不大,属于基础性题目.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
20.在某100mL混合酸中,HN03物质的量浓度是4mol•L-1,H2SO4物质的量浓度是2mol•L-1,向其中加入19.2g铜粉微热,待充分反应后,则被还原的HNO3物质的量为( )
| A. | 0.4mol | B. | 0.2mol | C. | 0.225mol | D. | 无法计算 |
2.乙苯催化脱氢制苯乙烯反应: 已知:1mol C-H键完全断裂时吸收热量412kJ,1mol C-C键完全断裂时吸收热量348kJ1mol C=C键完全断裂吸收热量612kJ,1mol H-H键完全断裂时吸收热量436kJ.上述反应的△H等于( ) kJ•mol-1.
已知:1mol C-H键完全断裂时吸收热量412kJ,1mol C-C键完全断裂时吸收热量348kJ1mol C=C键完全断裂吸收热量612kJ,1mol H-H键完全断裂时吸收热量436kJ.上述反应的△H等于( ) kJ•mol-1.
 已知:1mol C-H键完全断裂时吸收热量412kJ,1mol C-C键完全断裂时吸收热量348kJ1mol C=C键完全断裂吸收热量612kJ,1mol H-H键完全断裂时吸收热量436kJ.上述反应的△H等于( ) kJ•mol-1.
已知:1mol C-H键完全断裂时吸收热量412kJ,1mol C-C键完全断裂时吸收热量348kJ1mol C=C键完全断裂吸收热量612kJ,1mol H-H键完全断裂时吸收热量436kJ.上述反应的△H等于( ) kJ•mol-1.| A. | -124 | B. | +124 | C. | -288 | D. | +288 |
20.下列说法正确的是( )
| A. | 氯气有毒,所以不能用氯气对自来水进行消毒 | |
| B. | 液氯是纯净物,而氯水是混合物 | |
| C. | 碘化钾水溶液能使淀粉变蓝 | |
| D. | 在一个反应中,氧化剂和还原剂不可能是同一物质 |
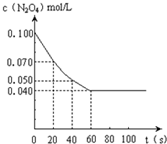 在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
在温度为373K时,将0.100mol无色的N2O4气体放入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)