题目内容
【题目】为测定某有机化合物A的结构,进行如下实验:
I. 分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况下),则该物质的实验式是__________.

(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为_______,该物质的分子式是_______.
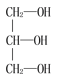
(3)根据有机化合物的成键特点,预测A的可能结构并写出结构简式__________.
II.结构式的确定:
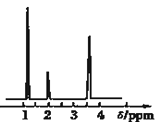
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.经测定,有机物A的核磁共振氢谱示意图如图②,则A的结构简式为_________.
【答案】C2H6O 46 C2H6O CH3CH2OH或CH3OCH3 CH3CH2OH
【解析】
(1)计算水、二氧化碳、氧气物质的量,根据原子守恒计算分子中C、H、O原子数目之比确定实验式。
(2)根据质荷比可知相对分子质量为46,结合最简式确定分子式。
(3)根据分子式书写可能的结构简式。
(4)有机物A的核磁共振氢谱中有3个吸收峰,说明有3种性质不同的H原子,结合分子式确定结构简式。
(1) 5.4gH2O的物质的量=![]() =0.3mol,则n(H)=0.6mol,8.8gCO2的物质的量
=0.3mol,则n(H)=0.6mol,8.8gCO2的物质的量![]() =0.2mol,则n(C)=0.2mol,6.72LO2的物质的量
=0.2mol,则n(C)=0.2mol,6.72LO2的物质的量![]() =0.3mol,由O元素守恒可知有机物中含有
=0.3mol,由O元素守恒可知有机物中含有![]() ,则分子中
,则分子中![]() ,故实验式为:C2H6O;
,故实验式为:C2H6O;
故答案为: C2H6O;
(2)由质谱图可知其相对分子质量为46,结合试验可知分子式为C2H6O;
故答案为:46;C2H6O;
(3)分子式为C2H6O的可能结构简式为:CH3CH2OH或CH3OCH3;
故答案为:CH3CH2OH或CH3OCH3;
(4)有机物A的核磁共振氢谱中有3个吸收峰,说明有3种性质不同的H原子,故A的结构为:CH3CH2OH;
故答案为:CH3CH2OH。

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案【题目】下列实验方案能达到相应实验目的的是
选项 | 实验目的 | 实验方案 |
A | 检验蔗糖水解生成葡萄糖 | 取适量蔗糖溶于盛有蒸馏水的试管中,滴入稀硫酸加热一段时间,冷却,滴入新制氢氧化铜悬浊液,加热至沸腾,观察有无砖红色沉淀 |
B | 实验室制备氢氧化铁胶体 | 向盛有25mL蒸馏水的烧杯中滴入5-6滴氯化铁饱和溶液,加热煮沸至溶液呈红褐色,停止加热 |
C | 比较AgCl、AgI的Ksp大小 | 向盛有10滴0.1mol/LAgNO3 溶液的试管中滴加0.1mol/LNaCl溶液至不再有沉淀生成,再滴加0.1mol/lKI溶液 |
D | 比较Mg、Al的金属性强弱 | 用导线连接镁和铝片,插入盛有氢氧化钠溶液的烧杯中,观察气泡 |
A. A B. B C. C D. D