题目内容
20.按括号内要求回答问题:(1)Fe2(SO4)3(写出电离方程式)Fe2(SO4)3=2Fe3++3SO42-
(2)氢氧化铜和盐酸反应(写出离子方程式)Cu(OH)2+2H+=Cu2++2H2O
(3)某一反应体系有反应物和生成物共5种物质:N2O、Zn(NO3)2、HNO3、Zn和H2O.写出该反应的化学方程式:4Zn+10HNO3=4Zn(NO3)2+N2O+5H2O
(4)除去Na2SO4 溶液中的Na2CO3杂质(写出对应的离子方程式)CO32-+2H+=CO2↑+H2O.
分析 (1)硫酸铁为强电解质,完全电离生成三价铁离子和硫酸根离子;
(2)氢氧化铜和盐酸反应生成氯化铜和水;
(3)锌与硝酸反应生成硝酸锌与氧化氮和水;
(4)碳酸钠与硫酸反应生成硫酸钠和二氧化碳和水.
解答 解:(1)硫酸铁为强电解质,完全电离生成三价铁离子和硫酸根离子,离子方程式:Fe2(SO4)3=2Fe3++3SO42-;
故答案为:Fe2(SO4)3=2Fe3++3SO42-;
(2)氢氧化铜和盐酸反应生成氯化铜和水,离子方程式:Cu(OH)2+2H+=Cu2++2H2O;
故答案为:Cu(OH)2+2H+=Cu2++2H2O;
(3)锌与硝酸反应生成硝酸锌与氧化氮和水,化学方程式:4Zn+10HNO3=4 Zn(NO3)2+N2O+5H2O;
故答案为:4Zn+10HNO3=4 Zn(NO3)2+N2O+5H2O;
(4)碳酸钠与硫酸反应生成硫酸钠和二氧化碳和水,离子方程式:CO32-+2H+=CO2↑+H2O;
故答案为:CO32-+2H+=CO2↑+H2O.
点评 本题考查了化学方程式、离子方程式的书写明确反应实质是解题关键,注意原子个数守恒、电荷数守恒规律,题目难度不大.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
10.近日来,全国安全事故频发,折射出人们对化学品与安全知识的极度缺乏,下列有关化学品与安全的说法或操作正确的是( )
| A. | 运液氯可用钢瓶装,车上应贴 标志.装运浓硫酸可用铝槽罐车,应贴 标志.装运浓硫酸可用铝槽罐车,应贴 标志 标志 | |
| B. | 冬天严禁在窗门紧闭的室内用煤饼炉取暖,因为生成的CO、CO2等容易引起中毒 | |
| C. | 洁厕灵和厨房清洁剂不 能混合使用,因为会反应生成Cl2引起中毒 | |
| D. | 患有胃溃疡的患者治疗胃酸过多,可用长期大量服用含Al(OH)3的胃药 |
5.某无色溶液中可能含有K+、Fe3+、Cu2+、SO42-、SO32-、CO32-、Cl-、Br-这几种离子中的若干种,依次进行下列实验,观察到的现象记录如下:①pH试纸检验,溶液的pH>7.②取少量原溶液,向溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成.③另取少量原溶液,向溶液中滴加足量氯水、无气体产生,再加入CCl4振荡,静置后CCl4层呈橙色,用分液漏斗分液.④向分液后的水溶液中加入Ba(NO3)2和HNO3溶液,有白色沉淀产生.⑤在滤液中加入AgNO3和HNO3的混合溶液有白色沉淀产生.则关于原溶液的判断中正确的是( )
| A. | 肯定不存在的离子是Fe3+、Cu2+、CO32-、Br- | |
| B. | 肯定存在的离子是K+、SO42-、SO32- | |
| C. | 无法确定原溶液中是否存在Cl-和CO32- | |
| D. | 若步骤④改用BaCl2和盐酸的混合溶液,则对溶液中离子的判断也无影响 |
12.下列说法正确的是( )
| A. | 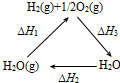 图中△H1=△H2+△H3 | |
| B. | 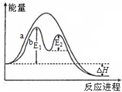 如图在催化剂条件下,反应的活化能等于E1+E2 | |
| C. |  如图表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 | |
| D. | 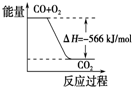 如图可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量 |
9.厨房中的化学知识很多,下面是有关厨房中的常见操作或者常见现象,其中发生的变化不属于氧化还原反应的是( )
| A. | 食物久置后,变质腐败产生异味 | |
| B. | 燃烧液化石油气为炒菜提供热量 | |
| C. | 食醋(CH3COOH)除去水瓶里的水垢[主要成分CaCO3和Mg(OH)2] | |
| D. | 烧菜用过的铁锅出现红棕色斑迹 |
 在一容积为2L的密闭容器内为加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0反应中NH3的物质的量浓度的变化的情况如图所示:
在一容积为2L的密闭容器内为加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0反应中NH3的物质的量浓度的变化的情况如图所示: